El paladio es un metal raro y precioso. Así, es más raro que la plata y dos veces más raro que el oro. Al igual que estos metales, el paladio tiene una superficie brillante y no se corroe fácilmente. El paladio se encuentra puro en la naturaleza, pero también tiene algunos minerales raros, como la braggita. De sus muchas aplicaciones, el uso principal del elemento es en convertidores catalíticos, de los tubos de escape de los vehículos. También, el cloruro de paladio, PdCl2, se usa en detectores de monóxido de carbono, CO. Debido a que es un metal precioso, se usa para hacer monedas conmemorativas en algunos países. El acero se puede fabricar con paladio para hacerlo más resistente a la corrosión. Estas aleaciones se utilizan para fabricar herramientas quirúrgicas e instrumentos musicales caros. El paladio a menudo se mezcla con oro para formar una aleación llamada oro blanco, que se usa en joyería. Algunas plumas estilográficas tienen puntas decoradas con paladio. El elemento también se usa en tiras reactivas de glucosa para glucómetros para medir el nivel en sangre.
Resumen de propiedades (Pd)
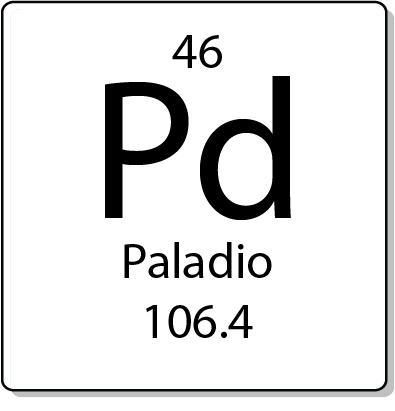
| Peso atómico | 106.42(1) |
| Descubridor (año) | Wollaston, William Hyde (1803) |
| Forma natural | sólido metálico (cúbico centrado en las caras) |
| Configuración electrónica | [Kr] 4d10 |
| Punto de fusión (ºC) | 1552 |
| Punto de ebullición (ºC) | 2927 |
| Abundancia en corteza terrestre (ppm) | 0.015 |
| Isótopo (abundancia) | 102Pd (1.02), 104Pd (11.14), 105Pd (22.33), 106Pd (27.33), 108Pd (26.46), 110Pd (11.72) |
| Densidad g/cm3 | 12.02 |
| Radio Van der Waals (pm) | 210 |
| Radio covalente (pm) | 130 |
| Electronegatividad (Pauling) | 2.2 |
| Entalpia de vaporización (kJ/mol) | 393.00 |
| Entalpía de fusión (kJ/mol) | 15.74 |
| Capacidad calorífica específica (J/g·K) a 25ºC y 1 atm | 0.25 |
| Conductividad térmica (W/cm·K) a 25ºC y 1 atm | 0.720 |
| Número de oxidación | +3, +2 |
| Afinidad electrónica (eV) | 0.56 |
| 1ª Energía de ionización (eV) | 8.3369 |
