Índice
¿Qué es el limoneno?
El limoneno es un producto natural que se extrae del aceite de la piel de las frutas cítricas (limón, naranja, etc.). Su fórmula molecular es C10H16 y masa molecular de 136.238 g·mol−1. Es un líquido incoloro o amarillo pálido. Su nombre IUPAC es el 1-metil-4-(prop-1-en-2-il)-ciclohexeno. Presenta el olor característico de naranjas y limones. Es un compuesto orgánico de la familia de los terpenos.
Aplicaciones
Su principal aplicación hoy día es como disolvente industrial biodebradable. Se utiliza también en Síntesis Orgánica para obtener otros compuestos químicos. En la Industria alimentaria (saborizante), farmacéutica, cosmética y además como disolvente de resinas, tintas, pigmentos, fabricación de adhesivos, etc.
Estructura química
El limoneno es un compuesto quiral y por tanto presenta dos enantiómeros. En consecuencia, existen dos isómeros ópticos: el enantiómero R-limoneno y el S-limoneno. También, se les denomina D-limoneno y L-limoneno (antiguamente se les denominaba dextro y levo, respectivamente). El limoneno dextrógiro (+) es un líquido aceitoso que puede extraerse fácilmente de la cáscara del limón y le confiere el olor característico a limón. Sien embargo, el limoneno levógiro (-) se extrae de la cáscara de la naranja y presenta un olor a naranja.
|
|
| Estructura 3D | Estructura 3D |
Propiedades fisicoquímicas
El R-limoneno se obtiene comercialmente a partir del limón y presenta una rotación quiral, [α]D, de 87–102°. El limoneno es un monoterpeno relativamente estable y se puede destilar sin descomposición, aunque a temperaturas elevadas se fragmenta para formar isopreno.
Tiene una densidad de 0.8411 g· mol–1 , con un punto de fusión de −74.35 ºC y un punto de ebullición de 176 ºC. Insoluble en agua y miscible con otros disolventes orgánicos como por ejemplo: benceno, cloroformo, eter, CS2 y CCl4. Presenta un índice de refracción nD = 1.4727.
Método de obtención
Biosíntesis
En la naturaleza, el limoneno se forma a partir de pirofosfato de geranilo, mediante la ciclación de un carbocatión de nerilo o su equivalente. El paso final implica la pérdida de un protón del catión para formar el alqueno.

Reacciones del limoneno
En Síntesis Orgánica, se utiliza limoneno como material de partida para obtener carvona. La carvona es un compuesto, de alto valor añadido, que se emplea en la industria farmacéutica y en la alimentaria (con propiedades anti-microbiales y anti-fúngicas).
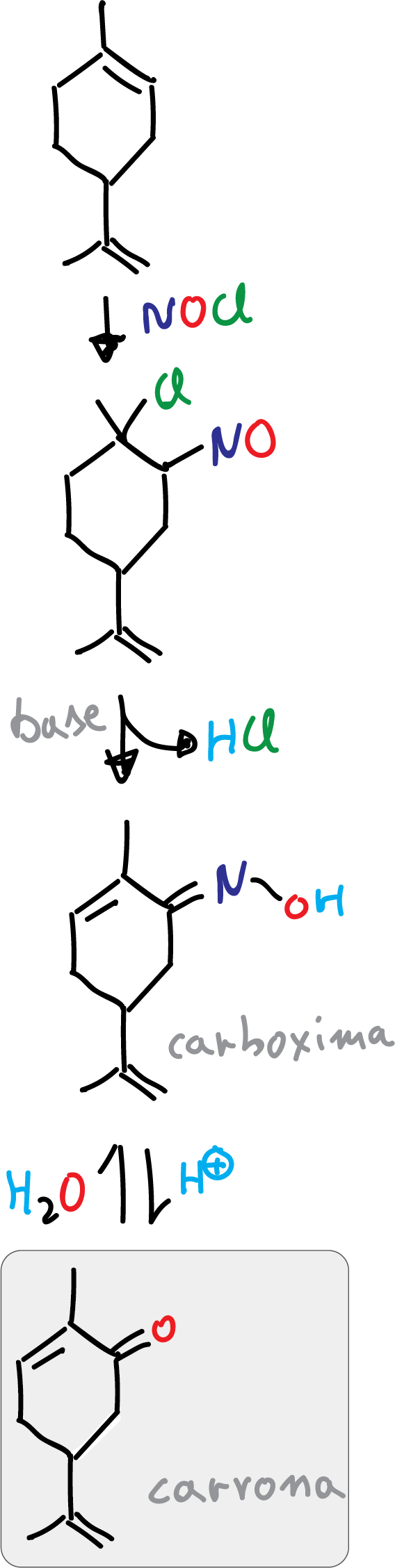
La síntesis consta de tres etapas, que comienza con la adición regioselectiva de cloruro de nitrosilo al doble enlace trisustituido. Posteriormente, este intermedio se convierte en la oxima con una base. Finalmente, la hidroxilamina obtenida se elimina para dar lugar a la carvona que presenta una cetona.
Por otro lado, el limoneno se oxida fácilmente en aire húmedo para producir carveol, carvona y óxido de limoneno. Con azufre, se deshidrogena a p-cimeno.
El limoneno se presenta comúnmente como enantiómero R, pero se racemiza a dipenteno a 300 °C. Cuando se calienta con ácido mineral, el limoneno se isomeriza al dieno conjugado α-terpineno (que también se puede convertir fácilmente en p-cimeno).
Es posible efectuar la reacción en uno de los dobles enlaces de forma selectiva. El HCl anhidro reacciona preferentemente en el alqueno disustituido, mientras que la epoxidación con mCPBA se produce en el alqueno trisustituido.
En otro método sintético, la adición de Markovnikov de ácido trifluoroacético al limoneno seguida de la hidrólisis del acetato resulta en el compuesto terpineol.
Video sobre el Limoneno
Clasificación GHS
Pictograma: Peligro



Frase H de peligro físico:
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.