Written by J.A. Dobado | Last Updated on 1 año
¿Qué es la cromatografía de capa fina (CCF)?
La cromatografía de capa fina (CCF) es una de las variantes más populares de la cromatografía líquido-sólido,[1] y sus usos más frecuentes son:
Índice
- Determinar los componentes de una mezcla.
- Determinar la identidad de dos sustancias.
- Seguir el curso de una reacción.
- Determinar las condiciones apropiadas para la separación de mezclas en cromatografía en columna (CC).
- Seguir el desarrollo de una columna de cromatografía.
Proceso de adsorción
La muestra se aplica sobre la capa y es adsorbida en la superficie del material por la acción de fuerzas electrostáticas (fuerzas de van der Waals, enlaces de hidrógeno, efectos inductivos, etc.). Luego, cuando la placa es expuesta a un flujo de disolvente por capilaridad, se inicia una competencia de uniones entre los sitios activos del adsorbente y la sustancia con el disolvente.
Adsorbentes
Los adsorbentes más utilizados en cromatografía de capa fina (CCF) son:
- Gel de sílice (SiO2): Se utiliza en el 80 % de las separaciones.
- Alúmina (Al2O3) (ácida, neutra o básica).
- Tierra silícea o Kieselguhr.
- Celulosa (nativa o micro-cristalina).
- Poliamida.
En la mayoría de los casos, en un laboratorio de Química Orgánica, se utiliza la gel de sílice como soporte. Estos adsorbentes se caracterizan por el tamaño de partícula (volumen de poro, diámetro de poro, área superficial, homogeneidad) y su pureza.
El adsorbente se deposita sobre una placa que actúa como soporte inerte y que suele estar fabricada en vidrio, aluminio y poliéster.
Aunque, cada vez está más extendido el uso de cromatofolios comerciales, también se pueden preparar las placas de cromatografía de capa fina (CCF) usando portaobjetos de vidrio. Se pueden preparar introduciendo dos portaobjetos juntos, limpios y secos, en una suspensión de gel de sílice al 35 % en AcOEt, que contiene CaSO4 como adhesivo.
La inmersión en la suspensión de adsorbente se lleva a cabo con ayuda de unas pinzas. La gel de sílice forma una película por cada una de las caras de los portaobjetos que queda expuesta a la suspensión. La evaporación del disolvente deja la placa lista para su uso.
Determinación del Rf
Para ayudar a identificar los productos que se encuentran en una mezcla, se suele utilizar el llamado factor de retención Rf (del inglés «ratio of front»). La forma de calcular el Rf se ilustra en la siguiente figura:
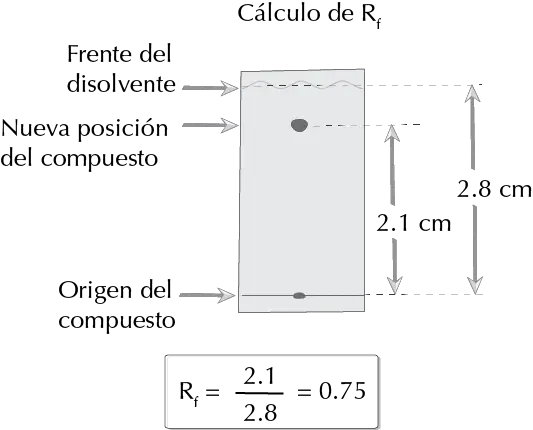
![]()
Descripción de materiales y procedimientos empleados en esta técnica
Los materiales que se usan en esta técnica son los que se detallan a continuación:
- Placas cromatográficas.
- Capilares y pipetas Pasteur.
- Eluyentes.
- Tanque de elución.
- Revelador.
Placa cromatográfica
Se usan como soporte del adsorbente láminas (cromatofolios) de vidrio, plástico o aluminio. Los tamaños de la placa para cromatografía de capa fina (CCF) convencional suelen ser de unas dimensiones de 20 x 20, 10 x 20 y 5 x 2 (en cm). Hay placas que contienen un indicador de fluorescencia (F254 o F366).[2]
Capilares y pipetas Pasteur
La muestra se aplica disuelta sobre la placa según que el objetivo sea preparativo o analítico. Con fines preparativos, la muestra se aplica disuelta y con ayuda de una pipeta Pasteur, es lo que se denomina aplicación en banda. Si lo que se pretende es realizar la técnica con fines analíticos, se aplica la muestra disuelta con ayuda de un capilar de vidrio.
En este caso se denomina aplicación por punto o mancha. La muestra se debe aplicar a una cierta distancia del borde de la placa. La altura y el lugar preciso donde se coloca la muestra se puede marcar con un lápiz, procurando no dañar el adsorbente.
Elección del eluyente
Se recomienda elegir un disolvente en el que los componentes de la mezcla presenten un Rf medio en torno a 0.3-0.5. La búsqueda del eluyente idóneo requiere probar con varios disolventes de diferente polaridad o con mezclas.
Cuando un compuesto eluye a Rf inferior a 0.2 o superior a 0.7, puede ocurrir que lo que parece un compuesto único sea en realidad una mezcla de varios. En estos casos, se debe cambiar a otro disolvente más o menos polar, respectivamente.
Para compuestos poco polares, que se desplazan desde el origen con mucha facilidad, se debe utilizar eluyentes apolares como el hexano. En el caso de compuestos de polaridad media, se aconseja utilizar mezclas hexano/acetato de etilo o hexano/éter dietílico en distintas proporciones. Los productos más polares, quedan muy retenidos en el adsorbente, requieren un disolvente más polar como mezclas CH2Cl2/MeOH en distintas proporciones.
Una forma de comprobar si el eluyente es el adecuado consiste en tomar una muestra de la mezcla que se va a cromatografiar y disolverla en la mezcla de disolventes elegida y pinchar con un capilar sobre una placa cromatográfica y observar el resultado de la difusión de la muestra.
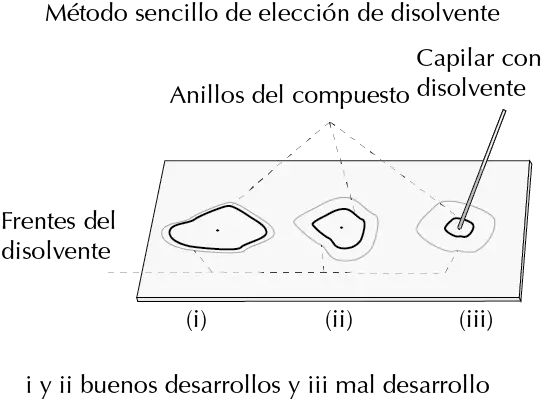
Si se detecta que las manchas correspondientes al producto forman aproximadamente un círculo que queda en la mitad del que forma el disolvente en la placa, la elección es la correcta, si por el contrario avanza muy próximo al frente del disolvente, o bien queda próxima al punto de origen, donde se aplicó la mancha, se debe buscar otro disolvente.
Tanque de elución (cubeta de cromatografía)
Es un recipiente cerrado que se utiliza para el desarrollo de placas de CCF. Su atmósfera está saturada de los vapores del eluyente. Existen, en el mercado, varios tipos de tanques.
Tanques de fondo plano con diversos diseños, tanques de doble compartimiento (con las ventajas frente a los anteriores de que disminuyen el consumo de disolvente y evita residuos, además de permitir saturar el ambiente con vapores de disolvente distinto al eluyente), etc.
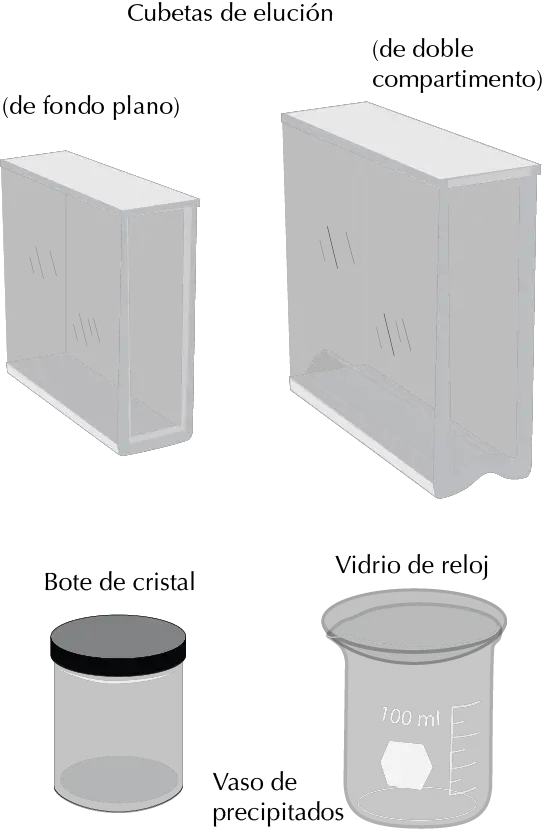
También, se usan frascos cerrados e incluso un vaso de precipitados tapado con un vidrio de reloj. El tanque se llena con el eluyente de forma que la altura del mismo no alcance la zona en donde se han situado los productos.
Suele ser una buena práctica introducir en el interior del tanque de elución un trozo de papel de filtro que llegue hasta la boca del tanque para que al ascender el eluyente por capilaridad, se sature el tanque de los vapores del eluyente. Esto facilita un correcto desarrollo de la placa. Cuando el frente de disolvente ha llegado al borde superior de la placa, se saca esta del tanque y se procede a su revelado.
Detección o visualización (revelado)
Si la muestra no es coloreada se necesitarán métodos que nos permitan visualizar los componentes presentes. Este procedimiento se conoce como revelado. Existen distintos métodos y entre los más utilizados destacamos los siguientes:
- Mediante una lámpara UV 254 nm con filtro: Cuando se usan placas con indicador UV si las sustancias tienen al menos un cromóforo, se observan manchas más oscuras en color verde claro y a veces manchas más brillantes, generalmente de color azul.

| ¡PELIGRO! «Nunca se debe mirar directamente la luz ultravioleta UV, ya que puede causar daños irreparables en los ojos.« |
- Métodos químicos: Existen muchos reveladores para CCF y los más comunes se listan a continuación:
- H2SO4/EtOH 50 %. Es un revelador universal y barato. Una vez pulverizada la placa de CCF, hay que calentarla bien con un secador de aire caliente o con una placa calefactora para que aparezcan las manchas, presentando estas colores oscuros.
- KMnO4 (3 g)/K2CO3 (10 g)/agua (300 ml). Considerado como revelador universal, solo incompatible con eluyentes que contengan aminas. La placa adquiere el color típico del permanganato y las manchas se muestran con tonalidades amarillas y/o pardas.
- Ácido fosfomolíbdico (10 g)/EtOH (100 ml). Aunque es caro, se aplica a la mayoría de las moléculas orgánicas.
- Ninhidrina (0.1 g)/ácido acético (2 ml)/acetona (100 ml). Se emplea principalmente para aminoácidos y compuestos nitrogenados.
- Yodo. Es uno de los reveladores más antiguos que se usa todavía para una gran variedad de moléculas orgánicas. Introduciendo durante unos minutos la placa en un tanque que contenga unos cuantos cristales de yodo, se observan manchas de tonos pardos que desaparecen cuando se saca la placa del tanque, por lo tanto se recomienda marcar las manchas con un lápiz para que tengamos una posterior referencia.
Los reveladores pueden usarse bien pulverizando la placa o bien por inmersión en un tanque con la disolución del revelador. En el caso de pulverizar las placas, se usan cabinas que permiten concentrar el revelador pulverizado sobre la placa y que suelen situarse en una vitrina de gases para que se extraigan los restos de aerosol del lugar de trabajo.

Procedimiento para una CCF analítica
- Preparar una disolución con una pequeña cantidad de la muestra.
- Para cromatofolios de 20 x 20 cm, cortarlos con ayuda de un cúter en placas de una altura aproximada de un tercio del cromatofolio y de una anchura variable en función del número de muestras que se vayan a pinchar.
- Trazar una línea con lápiz a aproximadamente 0.5 cm del borde de la placa y marcar con un punto los lugares en donde se pinchará la muestra con el capilar.
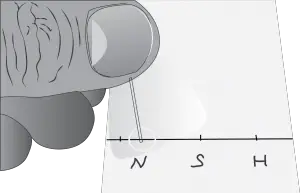
- Mojar el capilar en la disolución de la muestra y transferir el contenido a un punto de los marcados en la placa. Secar si fuese necesario con un secador de aire, para evitar que la disolución difunda a lo largo de la superficie de la placa antes de ponerla en el tanque.

- Introducir la placa en el tanque y dejar que el eluyente ascienda hasta el borde superior.
- Sacarla del tanque y proceder a su revelado.
Referencias y notas
- [1] Izmailov y Scraiber utilizaron en 1938 láminas de vidrio para colocar capas muy delgadas de alúmina y luego aplicaron extractos vegetales, originándose así la primera forma de cromatografía de capa fina (CCF) (en inglés «thin layer chromatograpy«, TLC). Egon Stanl (1956) dió el nombre de Cromatografía de Capa Fina (CCF). Estandarizó los procedimientos, equipos y adsorbentes popularizando esta técnica tan simple, eficiente y de bajo coste.
- [2] El número que aparece como subíndice indica la longitud de onda de excitación del indicador utilizado.
- Isac-García, J.; Dobado, J. A.; Calvo-Flores, F. G.; and Martínez-García, H. (2015). Experimental Organic Chemistry Laboratory Manual. Elsevier Science & Technology. ISBN: 978-0-12-803893-2
