Índice
Reacciones especiales de alquinos terminales
Reacciones con bases fuertes
Los alquinos terminales tratados con bases fuertes como el amiduro sódico en amoníaco líquido, forman aniones relativamente estables. Dichos aniones son nucleófilos que pueden usarse en reacciones de sustitución.
Una de las posibles aplicaciones es su empleo sobre haluros de alquilo primarios o secundarios para la preparación de alquinos sustituidos.
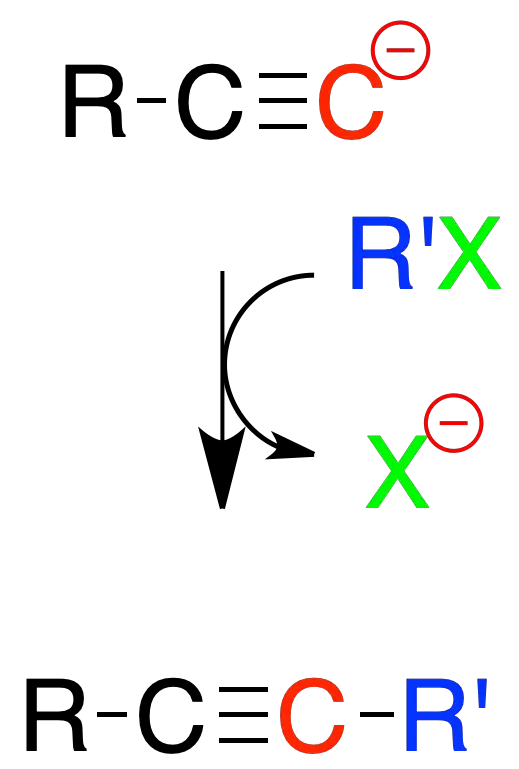
Formación de sales metálicas
Los alquinos terminales forman sales insolubles de cobre (I) o plata (I), lo cual permite distinguirlos de los alquinos disustituidos (donde no se forman estos precipitados).
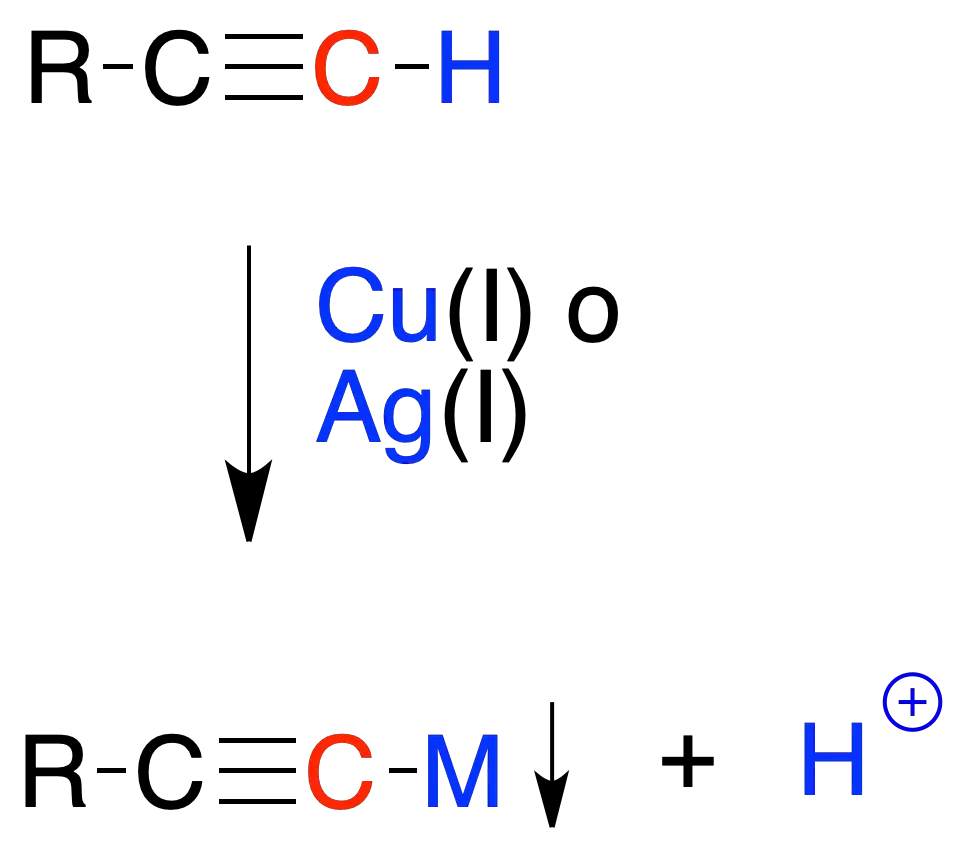
Reducción de alquinos
Hidrogenación catalítica
La hidrogenación catalítica de un alquino con un catalizador metálico (Pd, Pt, Rh, Ni, etc) conduce a la formación de un alcano de igual número de carbonos que el producto de partida.
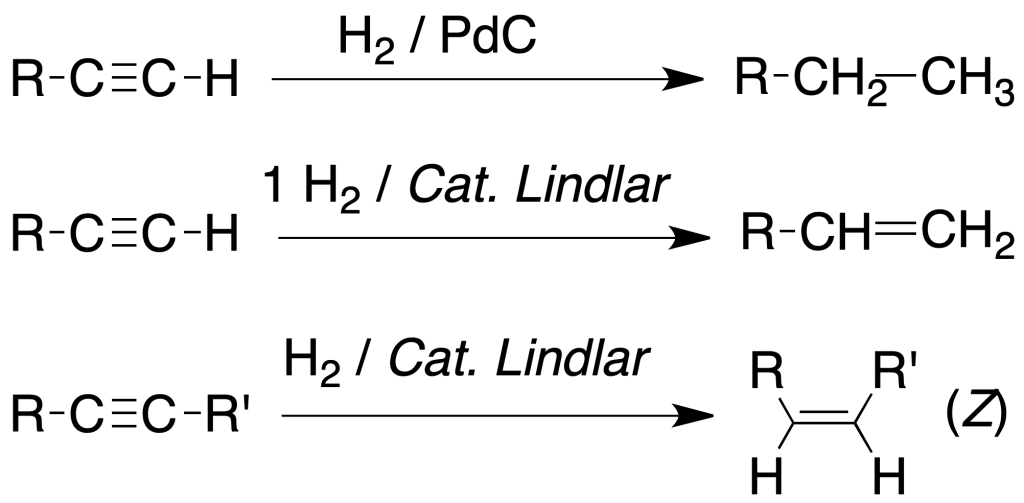
El catalizador suele ser un metal de transición finamente divido y en ocasiones, adherido a la superficie de un soporte inerte.
Sin embargo, usando 1 mol de hidrógeno, se produce un alqueno. Además, si se utilizan catalizadores modificados, es posible controlar la estereoquímica del proceso.
Por ejemplo, catalizadores parcialmente desactivados, como el catalizador de Lindlar (5% Pd / CaCO3 / Pb(AcO)2 / quinolina) o bien Pt / BaSO4, producen la hidrogenación incompleta de alquinos generando un alqueno de estereoquímica Z.
Reducción con metales
El tratamiento de un alquino con litio o sodio metálico en amoníaco líquido produce alquenos con estereoquímica E mediante un proceso de transferencia de electrones al sistema π del alquino.
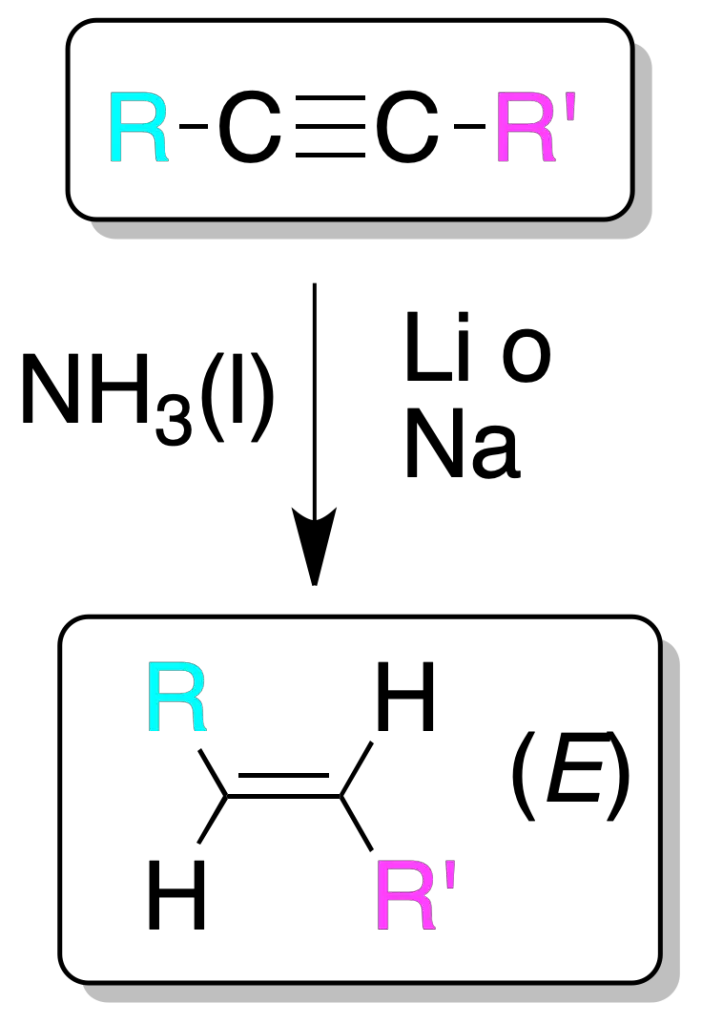
Adición electrofílica de alquinos
Al igual que los alquenos, los alquinos sufren adiciones electrofílicas.
Hidratación catalizada por ácido
Los alquinos adicionan una molécula de agua en presencia de un ácido mineral como H2SO4 y sales de Hg2+. Como resultado, se obtiene un enol que rápidamente evoluciona hacia el correspondiente compuesto carbonílico.
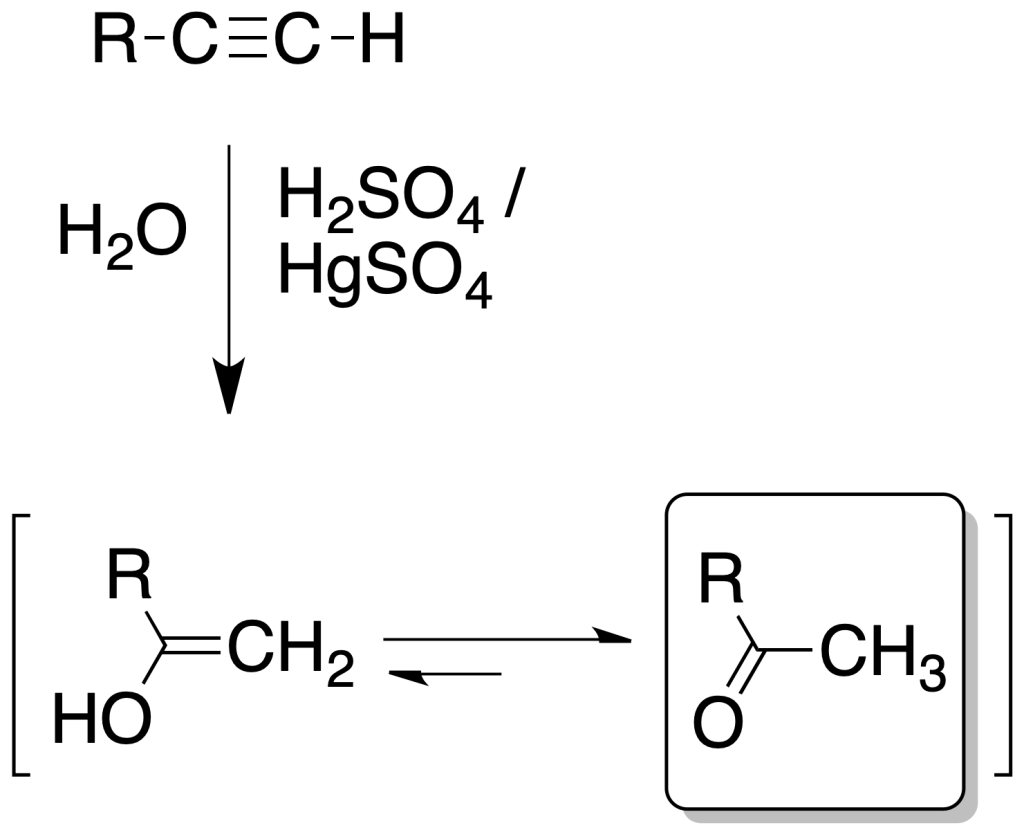
La adición de agua es de tipo Markovnikov, con lo cual en alquinos monosustituidos se obtienen cetonas.
En el caso de disustituidos da lugar a una mezcla de cetonas.
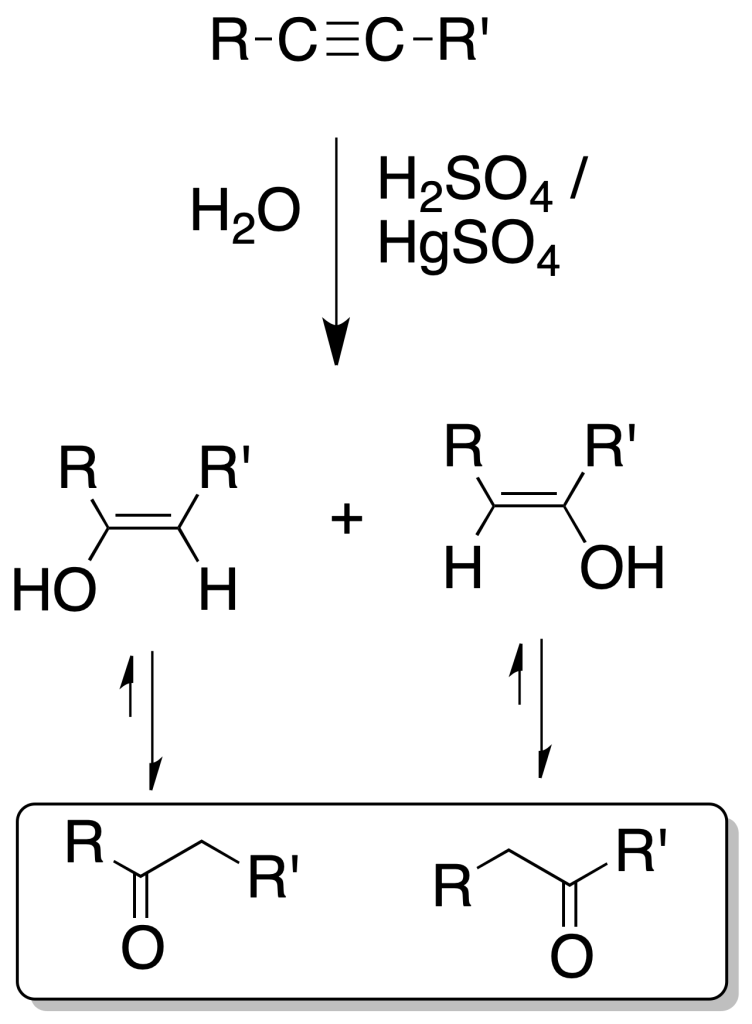
Hidroboración
La reacción de borano con alquinos lleva a la formación de un vinilborano, de manera que el átomo de boro se asocia al carbono menos sustituido (adición tipo anti-Markovnikov), predominado el factor estérico.
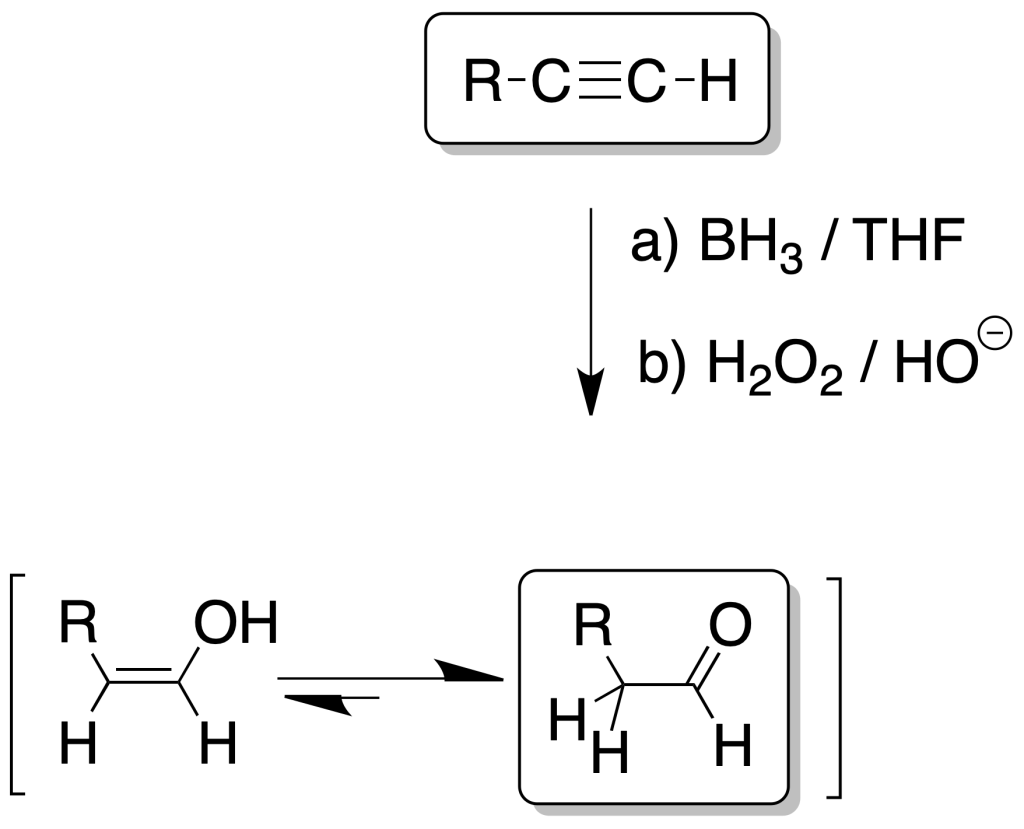
La oxidación con H2O2 del vinilborano produce un enol, que rápidamente evoluciona hacia el compuesto carbonílico de forma semejante a la reacción anterior.
Si el triple enlace del alquino de partida se encuentra en el extremo de una cadena carbonada, se obtiene un aldehído.
Adición electrófila de HX
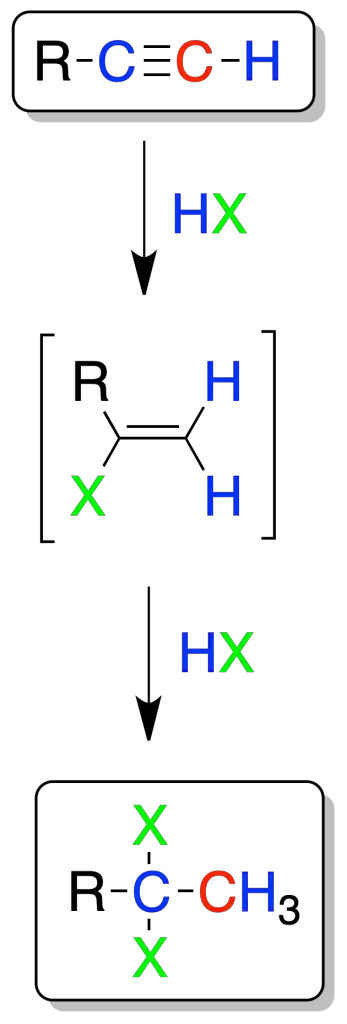
Esta reacción se realiza de forma secuencial, de manera que una primera molécula se adiciona con formación de un haluro de vinilo, y a continuación, la adición de una segunda molécula de HX.
La adición es de tipo Markovnikov y conduce a la formación de un dihaluro geminal.
En el caso de alquinos terminales, los átomos de halógeno quedan unidos al carbono secundario.
Adición de bromo
Los alquinos reaccionan con bromo para dar compuestos tetrahalogenados.
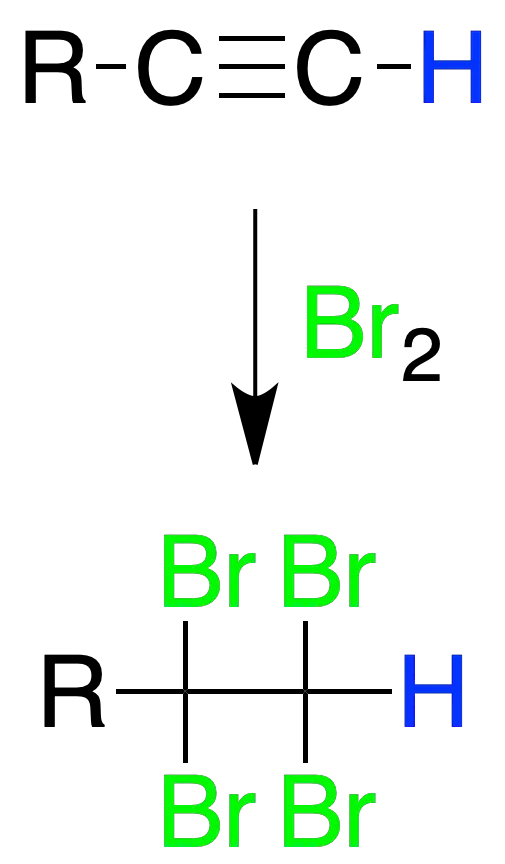
Si la reacción se realiza con cantidades equimoleculares de alquino y bromo, es posible aislar el derivado dibromado resultante de la adición de 1 mol de bromo.
La reacción es semejante a la adición de halógenos a doble enlaces. Se produce a través de un ión bromonio intermedio y es una adición de tipo anti.
Adición radicalaria a alquinos
La adición de HBr, a alquinos en presencia de iniciadores de radicales tiene lugar con una regioquímica contraria a la adición electrofílica (adición anti-Markovnikov).
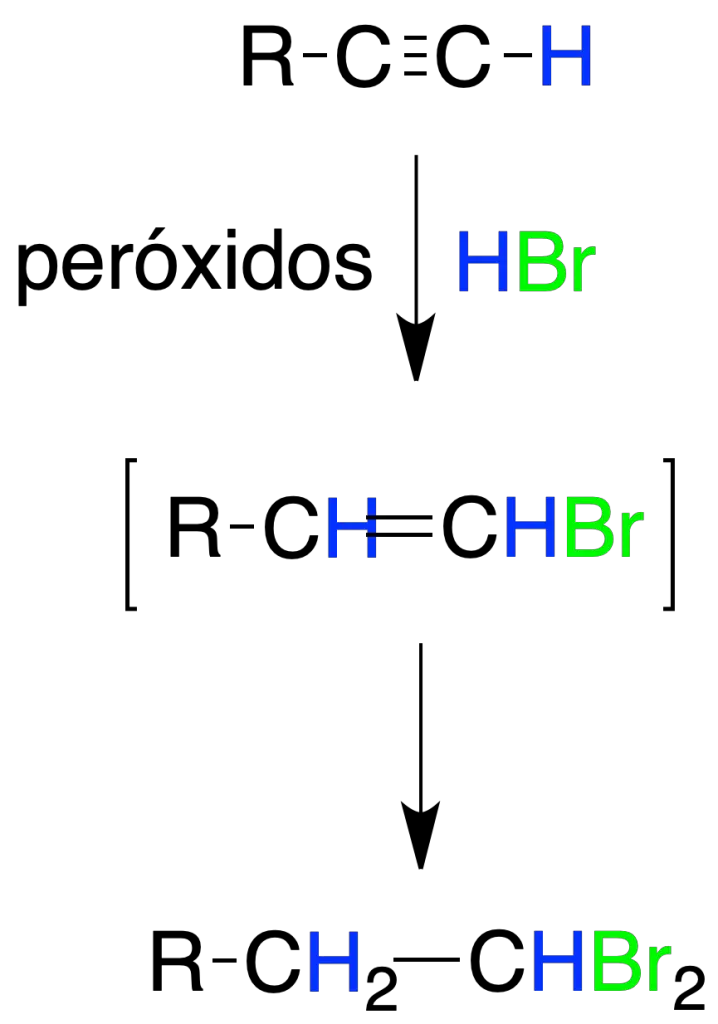
El mecanismo de reacción es de tipo radicalario, y en algunos casos es posible aislar el bromuro de vinilo obtenido por adición de 1 mol de HBr. Si hay un exceso de HBr se obtiene un dihaluro geminal.
Oxidación de alquinos
Ozonólisis
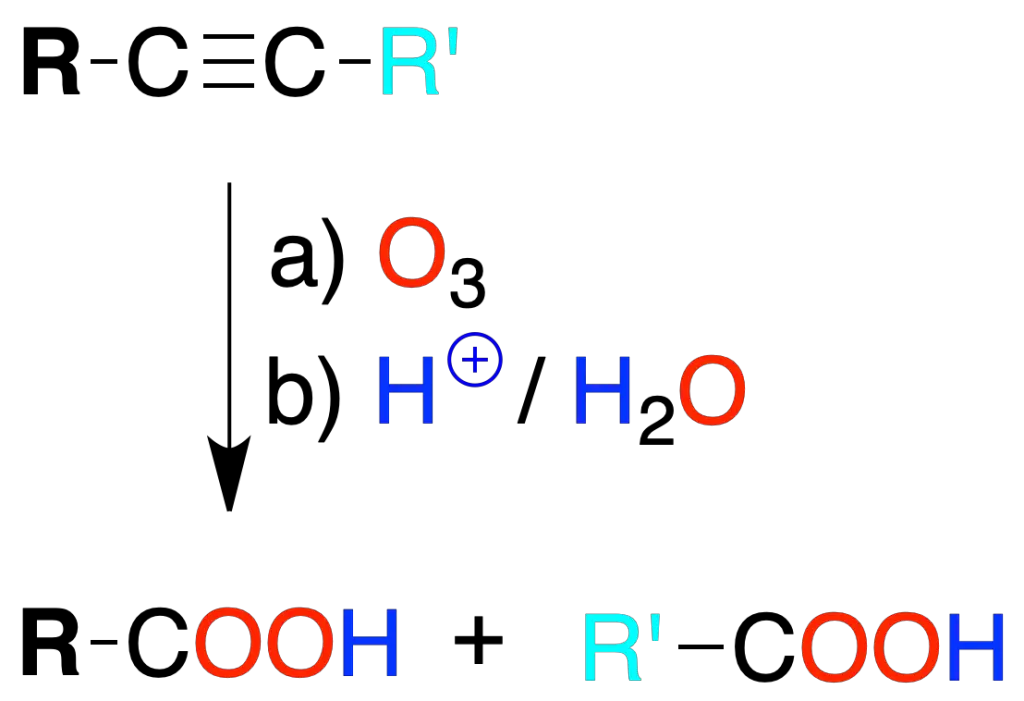
La reacción de un alquino con ozono, seguida de tratamiento con medio acuoso, conduce a la formación de ácidos carboxílicos. En el caso de un triple enlace terminal se produce CO2.
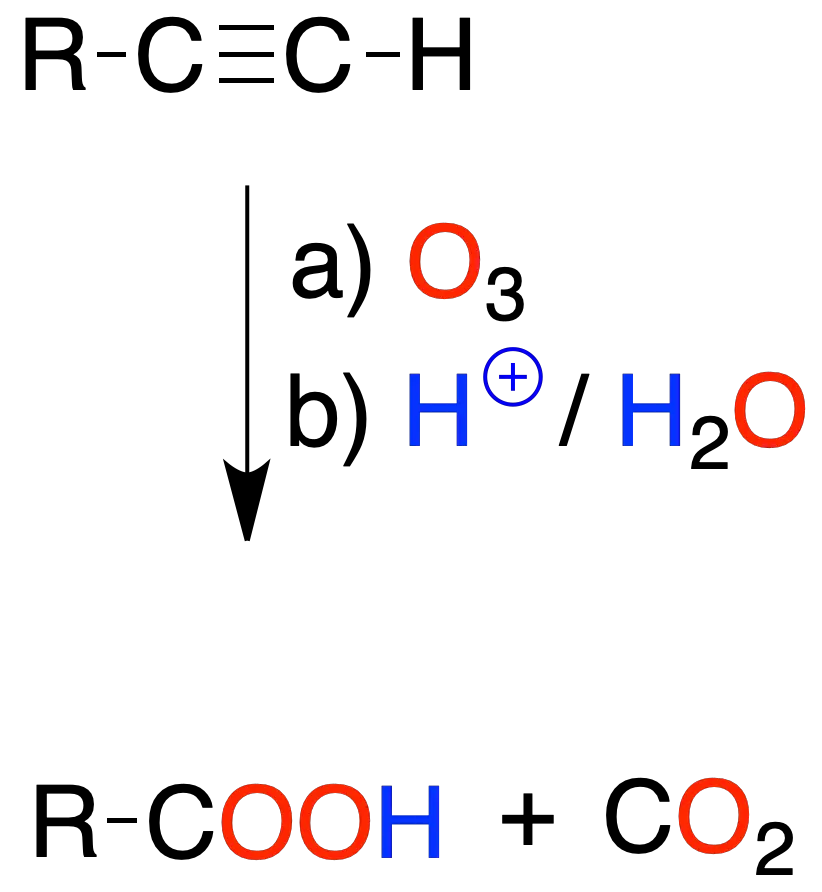
Al igual que en alquenos, la reacción se utiliza para caracterizar la estructura del alquino mediante el análisis de los fragmentos obtenidos.
Reacción con permanganato
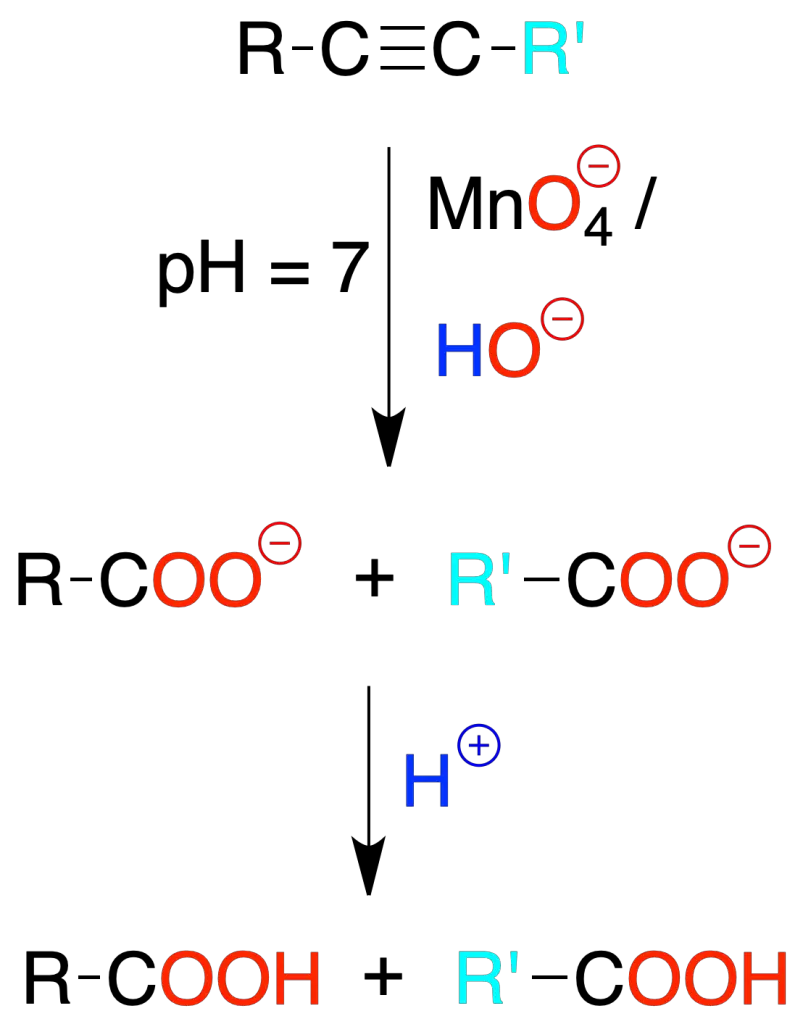
El permanganato potásico reacciona con alquinos en medio básico produciendo rotura oxidativa para dar la sal potásica de los ácidos carboxílicos. El ácido libre se obtiene acidificando.
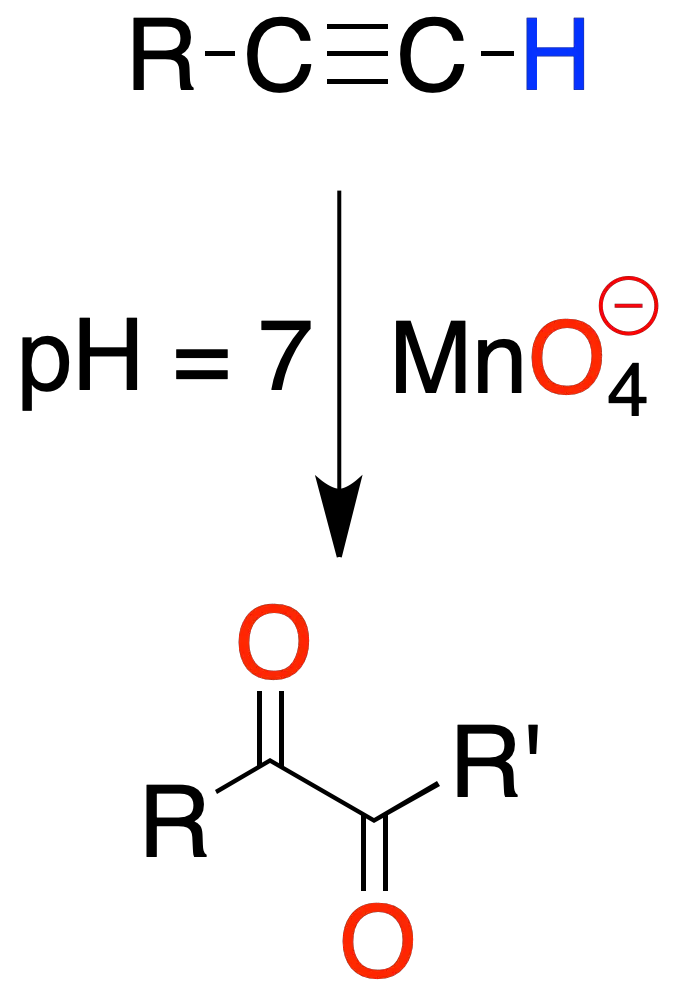
En alquinos disustituidos a pH neutro y en frío se obtiene un compuesto dicarbonílico, con dos grupos C=O sobre los carbonos que presentaban el triple enlace.
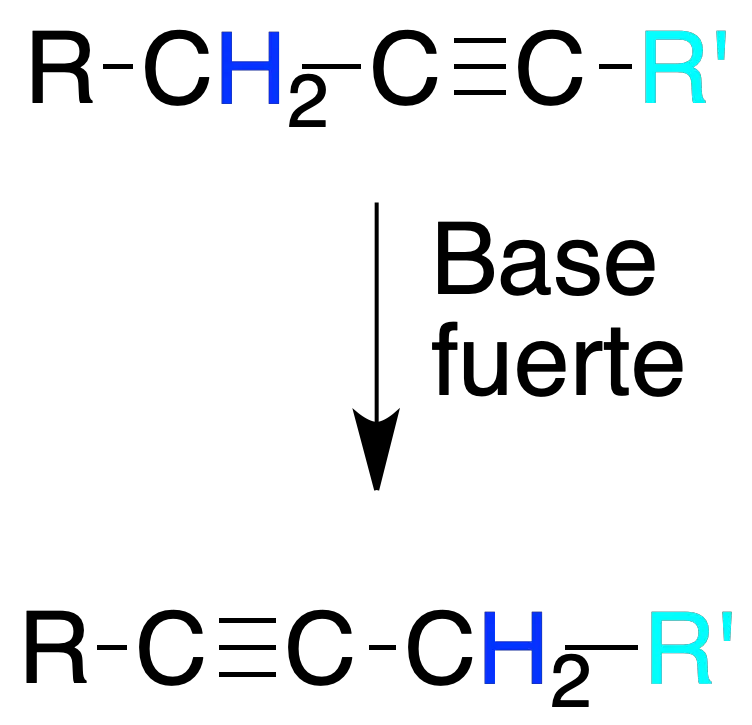
Isomerización de alquinos
Los alquinos disustituidos tratados con bases fuertes pueden dar otros alquinos isómeros por migración de los enlaces triples.
Video de Reacciones de Alquinos
Volver a la página de Síntesis y Reactividad de Compuestos Orgánicos.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.
