Índice
Objetivos
Realizar una síntesis estereoespecífica, así como mostrar la relevancia de los epóxidos (oxaciclopropanos) como intermedios versátiles en la Síntesis Orgánica.
Antecedentes
En este experimento, el trans-ciclohexano-1,2-diol se obtiene a partir del ciclohexeno, previo a la transformación de este último en trans-2-bromociclohexanol mediante un proceso estereoselectivo (adición anti a un doble enlace), seguido de la formación de un epóxido y posterior apertura de este.
Formalmente, la reacción produce la adición-anti del componente de ácido hipobromoso (HOBr) al doble enlace por reacción de ciclohexeno con N-bromosuccinimida (NBS) en un medio acuoso. El intermedio (ión bromonio) formado inicialmente reacciona con el agua, que es la especie más nucleófila presente (debido a que casi no es posible una concentración de iones bromuro).
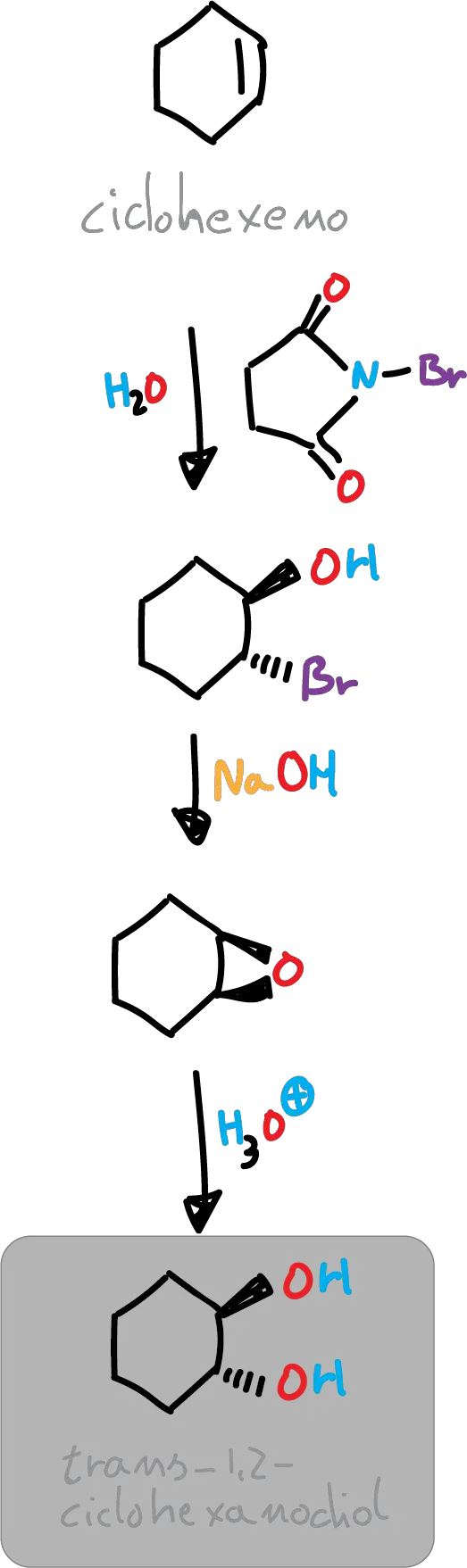
En este experimento, la bromohidrina intermedia no se aísla sino que se convierte inmediatamente en un epóxido. El tratamiento del trans-2-bromociclohexanol con una base conduce a la formación del epóxido correspondiente mediante un proceso de sustitución nucleofílica intramolecular. La disposición antiperiplanar disponible de los grupos OH y Br permite la formación de 1,2-epoxiciclohexano.
Cuanto mayor sea la reactividad de los epóxidos en comparación con los éteres acíclicos o cíclicos, cuanto mayor sea la tensión del anillo permite una ruptura relativamente fácil del enlace C-O.
La apertura del epóxido se realiza en medio ácido, por lo que se ejerce un control estérico sobre el proceso, ya que el epóxido se protona e induce el ataque del agua en la cara posterior del epóxido. El resultado es la formación de un diol trans.
Procedimiento experimental
A) Preparación de 2-bromociclohexan-1-ol
A un Erlenmeyer con un imán, agregue (en este orden): 7,6 ml de ciclohexeno, 20 ml de agua desionizada y 25 ml de THF. Coloque el matraz en un baño de hielo, sobre en una placa con agitación magnética y agite la reacción de 14.7 g de NBS en 40 ml de THF gradualmente durante aproximadamente 20 min. La temperatura de reacción no debe superar los 30 ºC. La temperatura se controla durante todo el proceso mediante la inserción de un termómetro en la reacción con cuidado para que no se golpeé con el imán. Después de la adición de NBS, mantener la agitación durante 30 min más. Trans finalizar los 30 min de reacción, se vierte el crudo de reacción en un embudo de decantación. Se agregan 30 ml de éter dietílico y 30 ml de salmuera. Se agita la mezcla y se decanta. Separar la capa orgánica (superior) y extraer la capa acuosa nuevamente con éter dietílico (2 x 20 ml). Combinar los extractos de éter dietílico y lavar de nuevo con salmuera (2 x 20 ml) para preparar una solución de trans-2-bromociclohexanol que se utilizará en el siguiente paso.
B) Preparación de 1,2-epoxiciclohexano
A un matraz de fondo redondo de 250 ml con tapones de vidrio esmerilado y adaptador Claisen (con un iman) o alternativamente a un matraz de dos bocas, se le agregan 25 ml de una solución de NaOH 5M. Montar un condensador de reflujo y agregar lentamente durante 40 min, desde el embudo de adición, una solución de 2-bromociclohexan-1-ol en éter, preparada en el paso anterior. Mientras se agita, mantener la temperatura de reacción a aproximadamente 40 ºC. Después de la adición, agite la mezcla durante 30 min. Cuando se complete la adición, transfiera la mezcla a un embudo de extracción. Separe las dos fases y seque la fase orgánica (superior) sobre gránulos de hidróxido de sodio, con agitación ocasional durante 15 min. Decantar la solución y eliminar el disolvente en el rotavapor. Destilar el residuo a presión atmosférica (124-134 ºC) y luego pesar y calcular el rendimiento de este paso.
C) Preparación de trans-ciclohexano-1,2-diol
En un matraz de fondo redondo de 100 ml, colocar 2 ml (1.95 g, 15 mmol) de 1,2-epoxiciclohexano. Ajustar las cantidades al resultado obtenido en la etapa anterior. Añadir 10 ml de agua y 1 ml de H2SO4 y agitar vigorosamente la mezcla durante 1 h (tapar el matraz). Durante este período de tiempo, observe que el matraz se calienta y que la mezcla de reacción se vuelve transparente. Después de agitar durante 1 h, ajuste el pH de la solución a 7 agregando gota a gota la solución de NaOH.
Extraer la solución acuosa con acetato de etilo (3 x 15 ml). Secar los extractos orgánicos sobre sulfato de sodio anhidro, eliminar el desecante por filtración por gravedad y concentrar en rotavapor hasta 1/3 del volumen. Luego, introduzca la disolución de acetato de etilo en un baño de hielo hasta que aparezca un sólido. Filtrar el sólido a vacío, secar con un flujo de aire, pesar y calcular el rendimiento.
Propiedades físico-químicas
La siguiente tabla recoge los datos de peso molecular (Mw), punto de fusión (P.F.) punto de ebullición (P.E.) y densidad de los reactivos y compuestos utilizados en este experimento de laboratorio.
| Name | Mw (g/mol) | M.p. (ºC) | B.p. (ºC) | Density (g/ml) |
| 1,2-Epoxiciclohexano | 98.14 | - | 129-130 | 0.97 |
| 2-Bromociclohexano-1-ol | 179.055 | 11.82 | 225.52 | 1.520 |
| Ciclohexeno | 82.14 | -104 | 83 | 0.779 |
| H2SO4 | 98.08 | 3 | - | 1.80-1.84 |
| NaOH | 40.00 | 318 | 1,390 | 2.130 |
| Tetrahidrofurano | 72.11 | -108.0 | 65-67 | 0.89 |
| trans-Ciclohexano-1,2-diol | 116.16 | 101-104 | - | - |
GHS pictogramas
Los pictogramas de peligro forman parte del Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos (GHS) y se recogen en la siguiente tabla para los compuestos químicos utilizados en este experimento.
| Name | GHS |
| 1,2-Epoxiciclohexano |    |
| 2-Bromociclohexano-1-ol | Véase MSDS |
| Ciclohexeno |    |
| H2SO4 |  |
| NaOH |  |
| Tetrahidrofurano |   |
| trans-Ciclohexano-1,2-diol | No peligroso |
Identificador Químico Internacional
Los identificadores IUPAC InChI key de los principales compuestos utilizados en este experimento se proporcionan para facilitar la nomenclatura y formulación de los compuestos químicos y la búsqueda de información en Internet de los mismos.
| 1,2-Epoxiciclohexano | ZWAJLVLEBYIOTI-UHFFFAOYSA-N |
| 2-Bromociclohexano-1-ol | AAMCLCZHZXKWRV-UHFFFAOYSA-N |
| Ciclohexeno | HGCIXCUEYOPUTN-UHFFFAOYSA-N |
| H2SO4 | QAOWNCQODCNURD-UHFFFAOYSA-N |
| NaOH | HEMHJVSKTPXQMS-UHFFFAOYSA-M |
| Tetrahidrofurano | WYURNTSHIVDZCO-UHFFFAOYSA-N |
| trans-Ciclohexano-1,2-diol | PFURGBBHAOXLIO-PHDIDXHHSA-N |
Volver a la página de prácticas de Síntesis Orgánica Avanzada.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.
