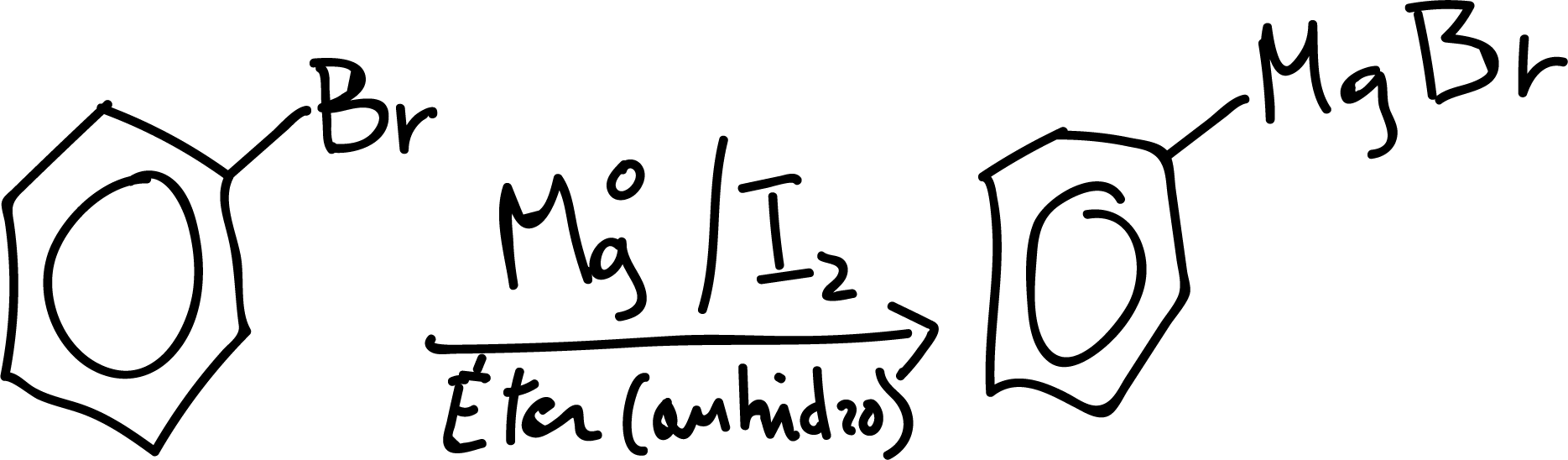Índice
Objetivo
Se familiariza al alumnado con las condiciones anhidras estrictas que conlleva la utilización de reactivos de Grignard, y en este caso para la obtención de ácido benzoico mediante la reacción de carbonatación de un reactivo de Grignard.
Antecedentes
Uno de los métodos más populares para formar enlaces C-C en síntesis orgánica es mediante el uso de reactivos de Grignard (Premio Nobel de Química en 1912). La formación de estos compuestos organometálicos implica la reacción de un haluro de alquilo, vinilo o arilo con magnesio e conlleva un cambio en la naturaleza electrónica del átomo de carbono, que cambia de electrófilo en el haluro a fuertemente nucleófilo en los compuestos de organomagnesio.
R-X + Mg → R-MgX
X= Cl, Br, I
Los compuestos de Grignard son altamente reactivos, reaccionan con agua, oxígeno, CO2, etc. Por tanto, estos compuestos deben prepararse en condiciones anhidras utilizando una atmósfera inerte. Tienen un carácter fuertemente nucleofílico (y básico) y producen adiciones a grupos carbonilo, con la formación de un nuevo enlace C-C, dando alcoholes cuya naturaleza depende del tipo de compuesto carbonilo de partida utilizado.
Un reactivo de Grignard se le considera como una unión de carbono o carbanión (la sal de magnesio de un hidrocarburo ácido). No obstante, es más exacto considerar que los reactivos de Grignard presentan un enlace C-Mg covalente altamente polar, y no un enlace iónico entre C⊖ y ⊕MgX.
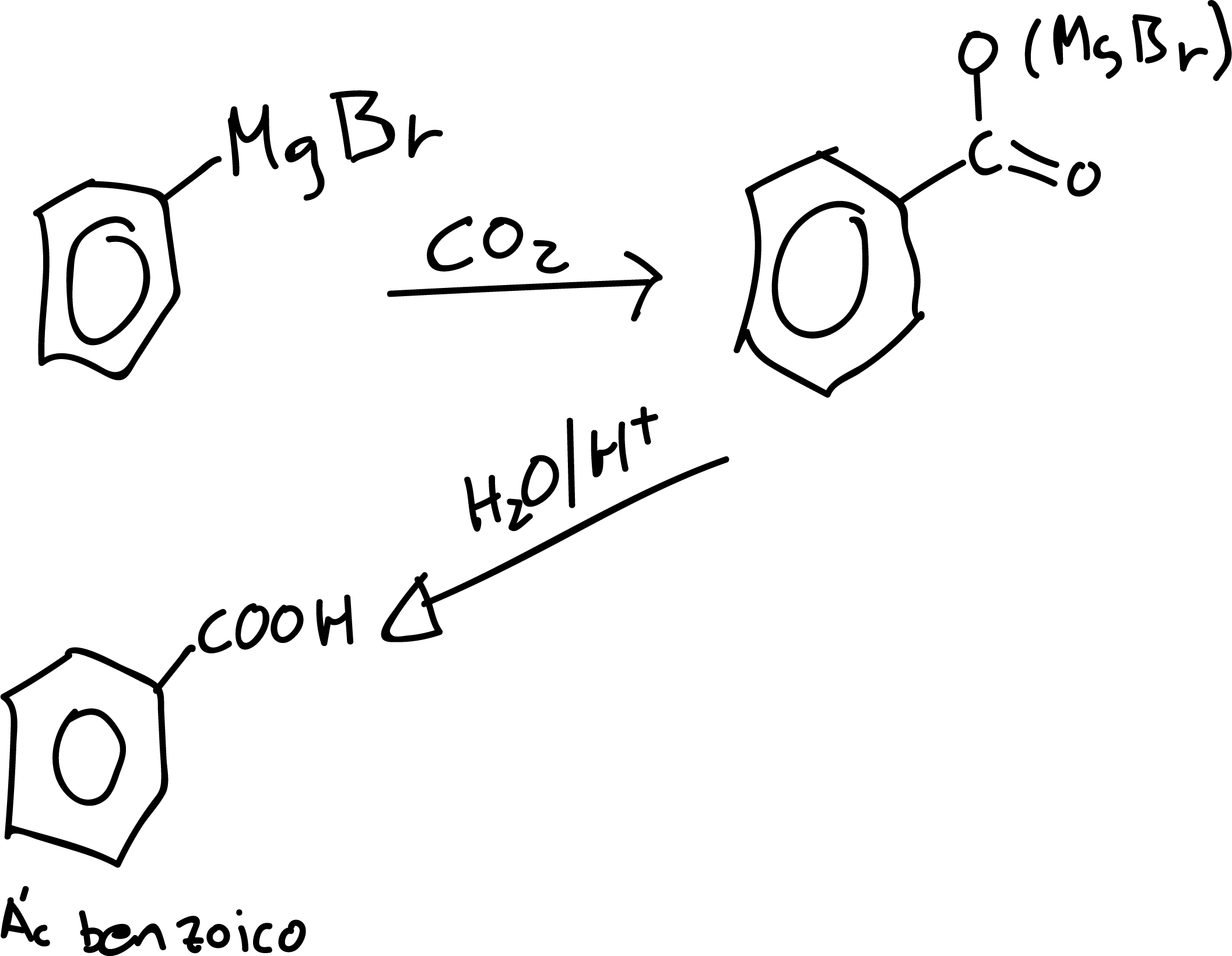
En esta práctica se va a proceder a sintetizar ácido benzoico a partir de bromobenceno convirtiendo este último en un reactivo de Grignard (Ph-MgX). El reactivo de Grignard se hace reaccionar a continuación con dióxido de carbono (CO2) gaseoso, para formar el ácido benzoico.
La síntesis de Grignard de un ácido carboxílico (R-COOH) se logra mediante un paso de carbonización burbujeando dióxido de carbono, CO2 gaseoso, en una solución en THF o éter dietílico del reactivo. En nuestro caso, se utiliza hielo seco molido (CO2 sólido) sobre el reactivo de Grignard. La ventaja de utilizar hielo seco es que no solo actúa como reactivo, sino como agente refrigerante.
Procedimiento experimental
Preparación del reactivo de Grignard (bromuro de fenilmagnesio)
Para poder llevar a cabo esta reacción con éxito es necesario que tanto los reactivos como el material utilizados estén completamente secos (utilizar estufa para el material si es necesario) y trabajar en condiciones de atmósfera inerte.
En un matraz de fondo redondo de 250 ml equipado con un refrigerante de reflujo, y un embudo de adición, bajo atmosfera inerte de argón, se colocan 2.4 g de magnesio Mg (en forma de virutas o limaduras). Posteriormente, se adicionan 30 ml de éter dietílico (anhidro) (se puede utilizar también THF).
Se añade una pequeña cantidad de activante (generalmente dibromoetano o yodo) y una vez activada la superficie del magnesio (las trazas de yodo se agregan para iniciar la reacción a temperaturas bajas sin tener que recurrir a un calentamiento inicial, pues la reacción luego es exotérmica.), se comienza a adicionar lentamenta 10 ml de bromobenceno anhidro.
Si la reación no se inicia inmediatamente se calienta en un baño de agua y se retira cuando la disolución comience a hervir (se observa la decoloración del yodo y aparición de turbidez).
Al ser la reacción exotérmica, se deja que transcurra la ebullición suave durante 30-40 min. En este punto, se corta el calentamiento para controlar la reacción (debido a que es exotérmica) hasta la formación del bromuro de fenilmagnesio.
Carbonatación del reactivo de Grignard
En un vaso de precipitados de 250 ml se coloca 15.14 g hielo seco triturado (CO2 sólido). Se vierte lentamente sobre el mismo, y utilizando agitación magnética, la solución de bromuro de fenilmagnesio preparada en la etapa anterior.
Se obtiene masa pastosa, que se continúa agitando hasta que todo el CO2 sólido haya sublimado.
A continuación, se añaden 50 ml de agua caliente, y se acidifica con HCl (dil.), para de esta forma poder disolver la sal de fenilmagnesio y obtener por precipitación el ácido benzoico. Se enfria, con un baño de hielo y se filtra a vacío. El ácido benzoico así obtenido, se puede recristalizar en agua.
Propiedades físico-químicas
La siguiente tabla recoge los datos de peso molecular (Mw), punto de fusión (P.F.) punto de ebullición (P.E.) y densidad de los reactivos y compuestos utilizados en este experimento de laboratorio.
| Name | Mw (g/mol) | M.p. (ºC) | B.p. (ºC) | Density (g/ml) |
| Ácido benzoico | 122.12 | 125 | 249 | 1.08 |
| Argón | 39.95 | -189.2 | -185.7 | - |
| Bromobenceno | 157.01 | -31 | 156 | - |
| CO2 | 44.01 | -78.5 | - | - |
| Éter dietílico | 74.12 | -116 | 34.6 | 0.71 |
| HCl | 36.46 | -30 | >100 | 1.200 |
| Yodo I2 | 253.81 | 113 | 184 | 4.930 |
| Magnesio | 24.31 | 648 | 1,090 | 1.740 |
| Bromuro de fenilmagnesio | 181.31 | - | - | - |
| Tetrahidrofurano | 72.11 | -108.0 | 65-67 | 0.89 |
GHS pictogramas
Los pictogramas de peligro forman parte del Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos (GHS) y se recogen en la siguiente tabla para los compuestos químicos utilizados en este experimento.
| Name | GHS |
| Ácido benzoico |   |
| Argón | No peligroso |
| Bromobenceno |    |
| CO2 |  |
| Éter dietílico |   |
| HCl |   |
| Yodo I2 |   |
| Magnesio |  |
| Bromuro de fenilmagnesio |    |
| Tetrahidrofurano |   |
Identificador Químico Internacional
Los identificadores IUPAC InChI key de los principales compuestos utilizados en este experimento se proporcionan para facilitar la nomenclatura y formulación de los compuestos químicos y la búsqueda de información en Internet de los mismos.
| Ácido benzoico | WPYMKLBDIGXBTP-UHFFFAOYSA-N |
| Argón | XKRFYHLGVUSROY-UHFFFAOYSA-N |
| Bromobenceno | QARVLSVVCXYDNA-UHFFFAOYSA-N |
| CO2 | CURLTUGMZLYLDI-UHFFFAOYSA-N |
| Éter dietílico | RTZKZFJDLAIYFH-UHFFFAOYSA-N |
| HCl | VEXZGXHMUGYJMC-UHFFFAOYSA-N |
| Yodo I2 | PNDPGZBMCMUPRI-UHFFFAOYSA-N |
| Magnesio | FYYHWMGAXLPEAU-UHFFFAOYSA-N |
| Bromuro de fenilmagnesio | NIXOIRLDFIPNLJ-UHFFFAOYSA-M |
| Tetrahidrofurano | WYURNTSHIVDZCO-UHFFFAOYSA-N |
Volver a la página de prácticas de Síntesis Orgánica.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.