Índice
¿Qué son los ácidos carboxílicos?
Los ácidos carboxílicos son compuestos que presentan, el grupo funcional -COOH (grupo carboxilo). Dependiendo del sustituyente al que este unido se clasifican en aromáticos o alifáticos.
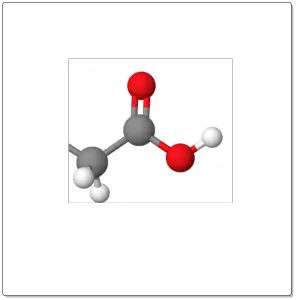
Si presenta más de un grupo carboxilo, se denominan ácidos dicarboxílicos (con dos), o policarboxílicos (más de dos).
Propiedades ácido-base
Los ácidos carboxílicos se disocian para dar un ión carboxilato RCOO⊖ y un protón H⊕, con valores de pKa del orden de 5 (ej. MeCOOH pKa = 4.7). Los valores de pKa o pKb del ácido o base conjugada se obtienen de la siguiente relación: pKa + pKb = 14.
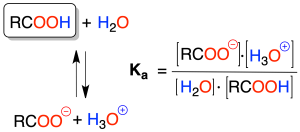
No son tan ácidos como los ácidos inorgánicos, pero sí mucho más que otros compuestos orgánicos; por ejemplo, el ácido acético es 1011 veces más ácido que los alcoholes.
Todo esto es debido a que la carga negativa está deslocalizada sobre varios átomos del grupo funcional -COO⊖ y por tanto hace que éste sea más estable que el alcóxido (O⊖) en el caso de los alcoholes.
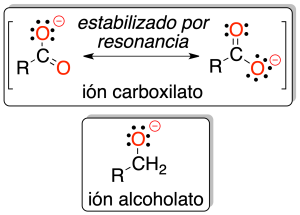
Por tanto, los ácidos carboxílicos reaccionan frente a bases para dar las correspondientes sales y agua. En el Apéndice C, se muestran los valores de pKa para los ácidos carboxílicos más comunes.
Formulación de ácidos carboxílicos
Siga el enlace para un resumen de las reglas de formulación y nomenclatura de ácidos carboxílicos.
Reacciones de ácidos carboxílicos
Además de las reacciones ácido base de los ácidos carboxílicos, en el apartado de reacciones de ácidos carboxílicos se describen las principales reacciones orgánicas de estos grupos funcionales y sus derivados.
Listado de ejercicios resueltos de ácidos carboxílicos
Siga el enlace para ver un listado de problemas resueltos sobre propiedades y reactividad de los ácidos carboxílicos y derivados.
Análisis de ácidos carboxílicos
Para distinguir un ácido carboxílico, insoluble en agua, de otros compuestos acídicos basta recurrir a las pruebas de solubilidad, pues son los únicos solubles en una disolución de NaOH/NaHCO3 (salvo algunos nitrofenoles). Los solubles en agua desprenden CO2 de la disolución de bicarbonato.
Otros compuestos que también dan CO2 son las sales de amina, los ácido sulfónicos y aquellos derivados de ácido que se hidrolizan fácilmente dando productos ácidos.
Para distinguir un ácido carboxílico, insoluble en agua, de otros compuestos acídicos basta recurrir a las pruebas de solubilidad, pues son los únicos solubles en una disolución de NaOH/NaHCO3 (salvo algunos nitrofenoles).
Presentan una banda de OH muy ancha y característica en el espectro de IR, además de una banda carbonílica cercana a los 1700 cm-1.
Los ácido carboxílicos se pueden caracterizar mediante la formación de los siguientes derivados:
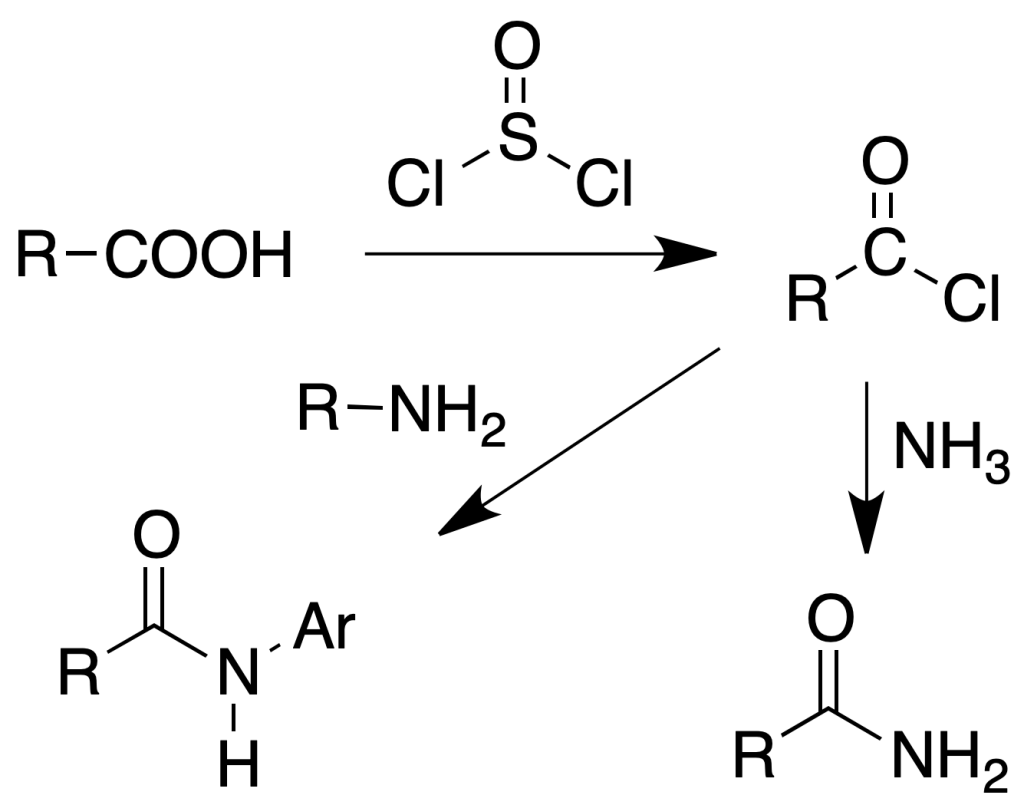
Formación de amidas
Procedimiento: En un matraz de 25 ml, equipado con reflujo y tubo de cloruro cálcico se colocan 100 mg del ácido (o de su sal sódica) y se le añaden 4 ml de cloruro de tionilo. Se hierve la mezcla suavemente durante 30 min y a continuación se vierte la mezcla sobre 15 ml de amoniaco concentrado enfriado con hielo. La amida precipitada se recoge por filtración.
Si en lugar de la amida se quiere preparar anilida o p-toluida se destila el exceso de cloruro de tionilo (p.e. = 78 ºC). Se disuelve el cloruro de ácido en 5 ml de benceno y se le añade una disolución de 2 g de la amina en 15 ml de benceno.
Se sacude la mezcla de reacción con 5 ml de HCl diluído (para eliminar el exceso de anilina) y se decanta. La capa de benceno se lava con 5 ml de agua, se elimina el disolvente y la anilida se recristaliza de agua o de EtOH/H2O.
Ésteres de fenacilo
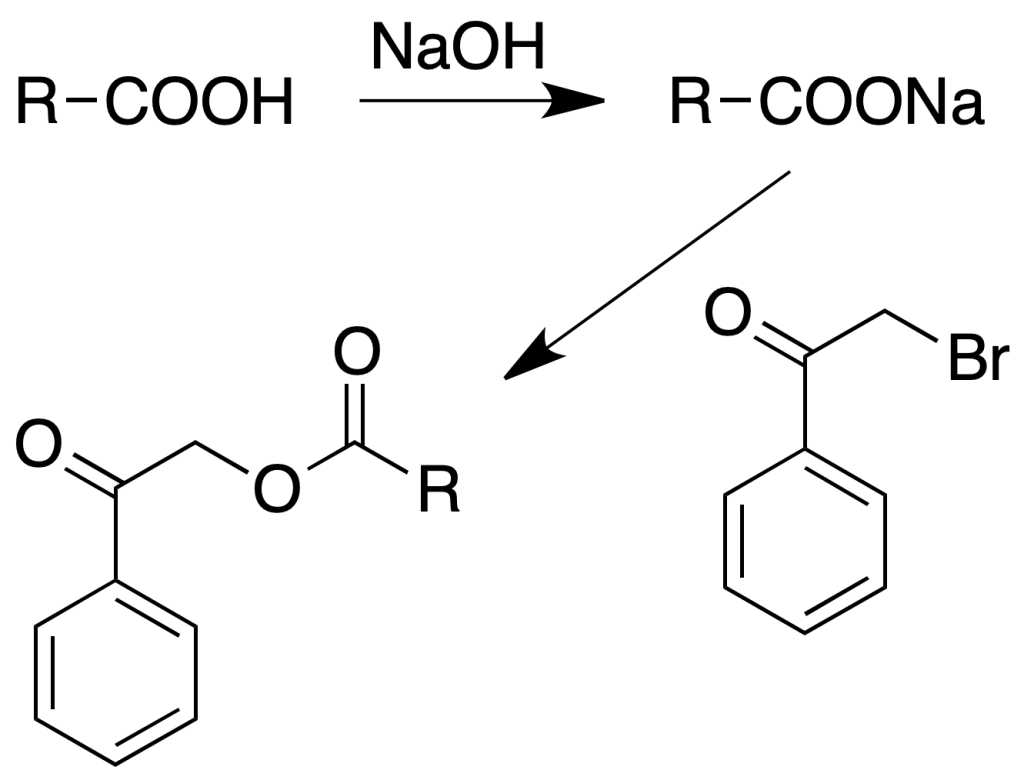
Procedimiento: Colocar en un matraz provisto de reflujo 150 mg de ácido y 1 ml de agua. Añadir una gota de fenolftaleina y neutralizar con NaOH al 10 % hasta color rosado. Añadir una o dos gotas de HCl diluído para que desaparezca el color.
Añadir una disolución alcohólica del bromuro de fenacilo (150 mg en unos 6 ml de alcohol).
Hervir la disolución a reflujo durante al menos 2 h; enfriar, añadir 1 ml de agua y raspar con una varilla para inducir la cristalización.
Filtrar el éster sólido, lavándolo con disolución de carbonato sódico al 5 % y después varias veces con agua fría.
Si se tratase de la sal sódica disolver unos 150 mg de ella en agua, poner una gota de fenolftaleina y ajustar el pH como en el caso anterior.
Volver a la página de análisis de grupos funcionales.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.
