Índice
Características comunes de aldehídos y cetonas
Los aldehídos y las cetonas poseen reacciones características comunes debido a la presencia en ambas del grupo carbonilo, pero también presentan reacciones diferenciadas debido a la propiedad que poseen los aldehídos de oxidarse a ácidos por la acción de oxidantes suaves. El análisis de aldehídos y cetonas se centra en la presencia del grupo carbonilo se detecta por la aparición de una banda de absorción en el espectro de IR (que suele ser la más intensa del espectro) en la región de 1650 a 1850 cm-1. Se diferencian de los ésteres por la ausencia de dos bandas intensas en la región de 1050 a 1250 cm-1 que aparecen en estos.
Combinación bisulfítica
Esta es una reacción característica del análisis de aldehídos y cetonas, ya que la dan todos los aldehídos y la mayoría de las cetonas a excepción de las impedidas estéricamente.
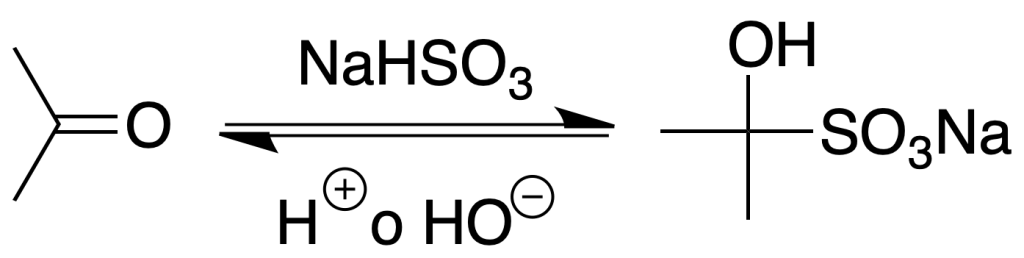
Procedimiento: Agitar vigorosamente la mezcla que contiene el aldehído o la cetona con una disolución saturada de hidrogenosulfito sódico. Se elevará la temperatura debido a que la reacción de adición es exotérmica. Recoger el material cristalino, lavarlo con EtOH y con éter etílico y dejar secar. Se puede descomponer el compuesto de adición con una disolución de carbonato sódico al 10 % o con HCl diluído.
La aparición de un precipitado demuestra la presencia de grupo carbonilo.
Formación de la 2,4-dinitrofenilhidrazonas
Aldehídos y cetonas se identifican por la formación de 2,4-dinitrofenilhidrazonas por reacción con 2,4-fenilhidrazina, obteniéndose un precipitado. Si el producto cristalino es de color amarillo, es indicativo de un compuesto carbonílico saturado, si se obtiene un precipitado de color naranja indica la presencia de un sistema α,β-insaturado y si lo que se obtiene es un precipitado de color rojo denota la presencia de una cetona o un aldehído aromático.
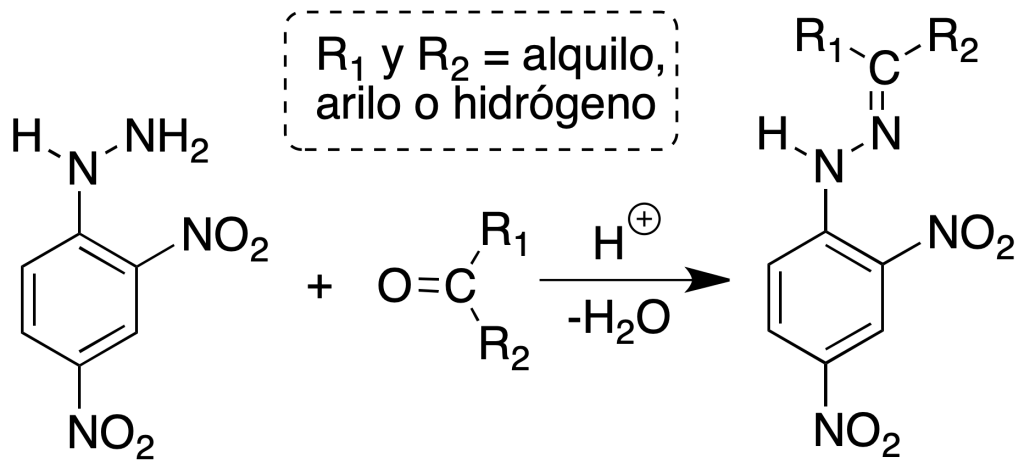
Preparación del reactivo: Se disuelven 3 g de 2,4-dinitrofenilhidrazina en 15 ml de H2SO4 concentrado. Añadir esta disolución, con agitación, sobre otra de 20 ml de agua y 70 ml de EtOH. Mezclar ambas disoluciones y filtrar.
Procedimiento: A un tubo de ensayo conteniendo 1 ml de reactivo se añade una gota del compuesto carbonílico si es líquido o unos 50 mg si es sólido disuelto en EtOH. Agitar vigorosamente la mezcla. Si no se forma inmediatamente un sólido, dejar reposar 15 min.
La formación de un precipitado entre amarillo y rojo se considera un resultado positivo. Determinar el punto de fusión teniendo en cuenta la posibilidad de que se trate de 2,4-dinitrofenilhidrazina (punto de fusión = 198 ºC).
Diferencias de aldehídos con respecto a cetonas
Reactivo de Tollens
El reactivo es una disolución amoniacal de AgOH que se prepara en el momento de su utilización.
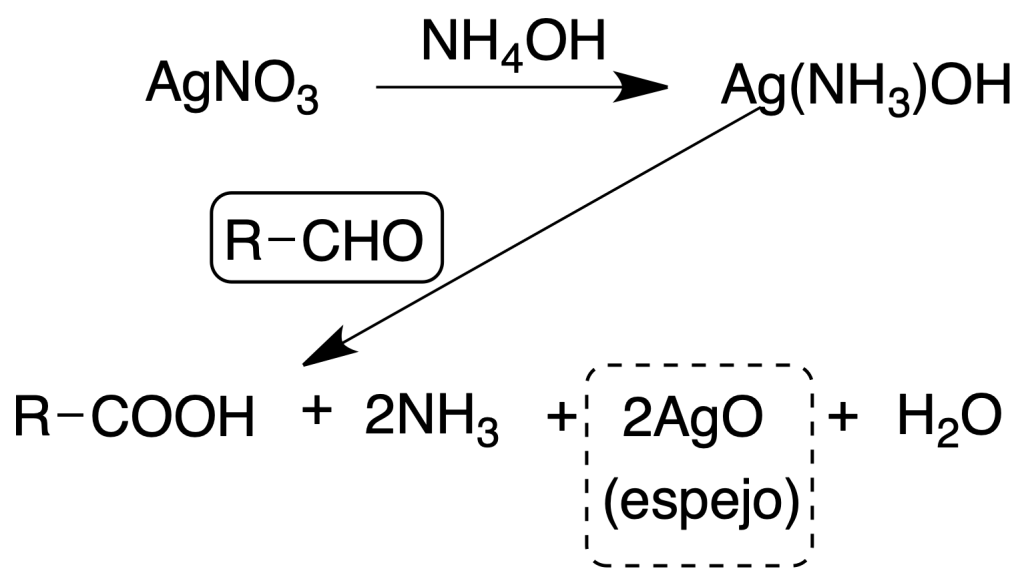
Las cetonas no dan esta reacción, excepto las hidroxicetonas y las 1,2-dicetonas que son reductoras y algunos compuestos nitrogenados como las hidrazinas, hidroxilaminas, aminofenoles, que se diferencian de estos fácilmente.
Procedimiento: Preparar dos soluciones.
- Disolución A: Se disuelven 3 g de nitrato de plata en 30 ml de agua.
- Disolución B: Una disolución de NaOH al 10 %.
Cuando se necesite el reactivo, mezclar en un tubo de ensayo limpio 1 ml de cada una de ambas disoluciones (A y B) y añadir gota a gota una disolución diluida de amoniaco hasta total disolución del óxido de plata. Adicionar unas gotas de una disolución diluida del compuesto a la mezcla anterior. En un ensayo positivo, la plata se deposita en forma de espejo en las paredes del tubo ya sea en frío o después de calentar en un baño de agua caliente. Para lavar el tubo y eliminar la plata depositada, hacerlo con HNO3 diluído.
Reactivo de Fehling
Diferencias de cetonas con respecto a aldehídos
La reacción más utilizada es la del yodoformo. Se emplea para la identificación de metilcetonas.
![]()
Es necesario indicar que además de estas también la dan positiva aquellas sustancias que puedan dar metilcetonas por oxidación, además del EtOH y acetaldehído.
Ensayo de yodoformo para metilcetonas
Consiste en la rotura del compuesto carbonílico por el enlace metil-carbonilo y la oxidación posterior a ácido carboxílico.
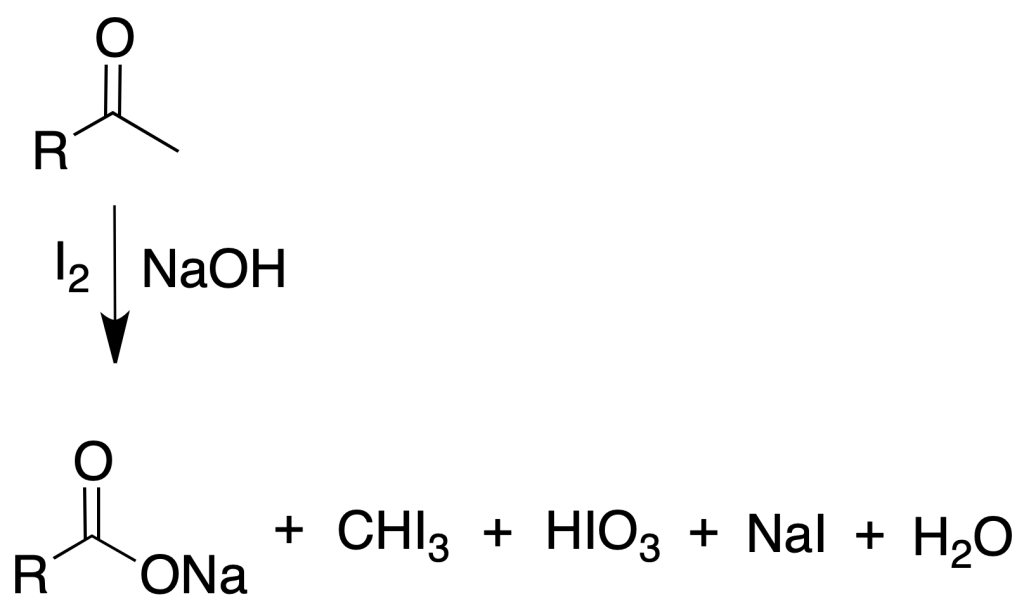
Procedimiento: Se prepara el reactivo por disolución de 20 g de yoduro potásico y 10 g de yodo en 100 ml de agua. Disolver 5 o 6 gotas del compuesto (aprox. 100 mg) en 2 ml de agua. Añadir si fuera necesario dioxano para disolver la muestra.
| ¡PELIGRO! «Realizar el ensayo en vitrina y empleando guantes.» |
Añadir 1 ml de NaOH al 10 % y el reactivo I2 / I–, gota a gota y con agitación, hasta que persista el color oscuro del yodo. Dejar reposar durante algunos minutos. Si no aparece precipitado calentar en un baño a 60 ºC, si desaparece el color al calentar, añadir más reactivo, hasta que permanezca el color.
A continuación, se adicionan unas gotas de disolución de hidróxido sódico, se diluye con 4 ml de agua y se deja reposar durante 15 min. Un resultado positivo vendrá indicado por la aparición de un precipitado amarillo (punto de fusión = 119-121 ºC) con característico olor medicinal.
Caracterización de aldehídos y cetonas
Fenilhidrazonas
Procedimiento: Colocar en un tubo de ensayo 100 mg de compuesto carbonílico, 4 ml de MeOH y 4 gotas de fenilhidrazina. Hervir la mezcla durante 1 min, añadir una gota de ácido acético glacial y volver a hervir durante 3 min.
Añadir gota a gota agua fría hasta que aparezca una turbidez permanente. Enfriar, recoger los cristales y lavarlos con 1 ml de agua que contenga ácido acético. Recristalizarlos de MeOH caliente añadiendo agua gota a gota hasta punto de turbidez.
2,4-Dinitro- y p-nitro-fenilhidrazonas
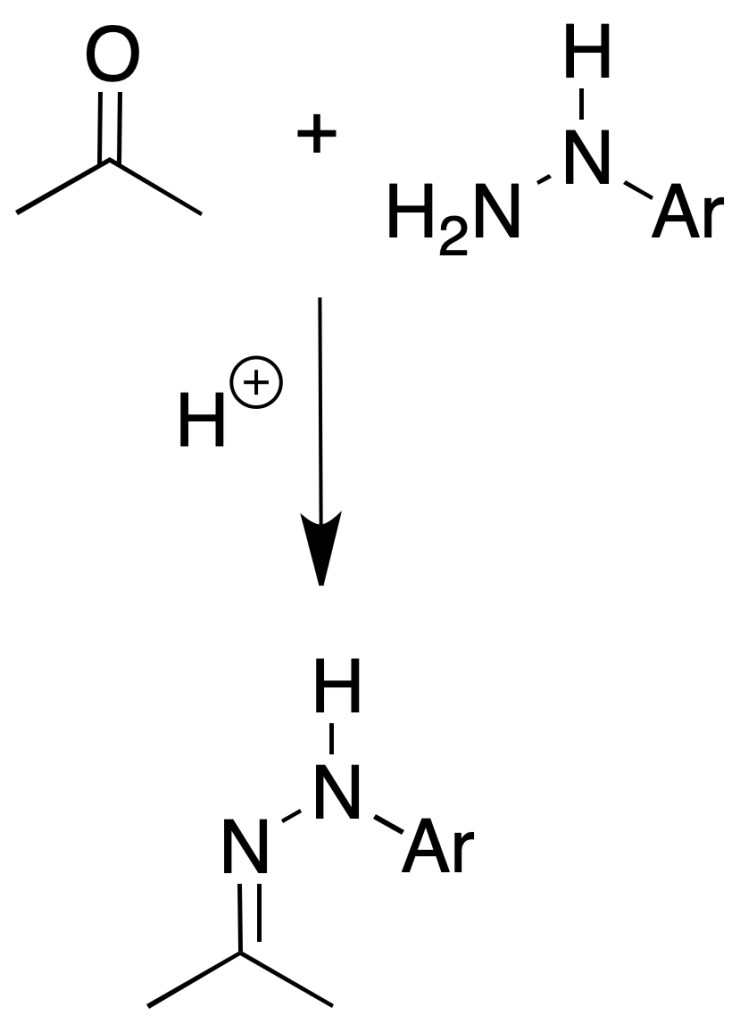
Procedimiento: Colocar 100 mg de la nitrofenilhidrazina en un tubo de ensayo o Erlenmeyer con 10 ml de MeOH. Añadir 5 gotas de HCl concentrado y calentar si es necesario para completar la disolución. Disolver unos 100 mg del compuesto en 1 ml de MeOH y añadirlo al reactivo.
Calentar la mezcla en un baño de vapor durante 2 min y dejar reposar durante 20-30 min. Para asegurarse la cristalización es aconsejable la adición de agua hasta turbidez persistente.
Semicarbazonas
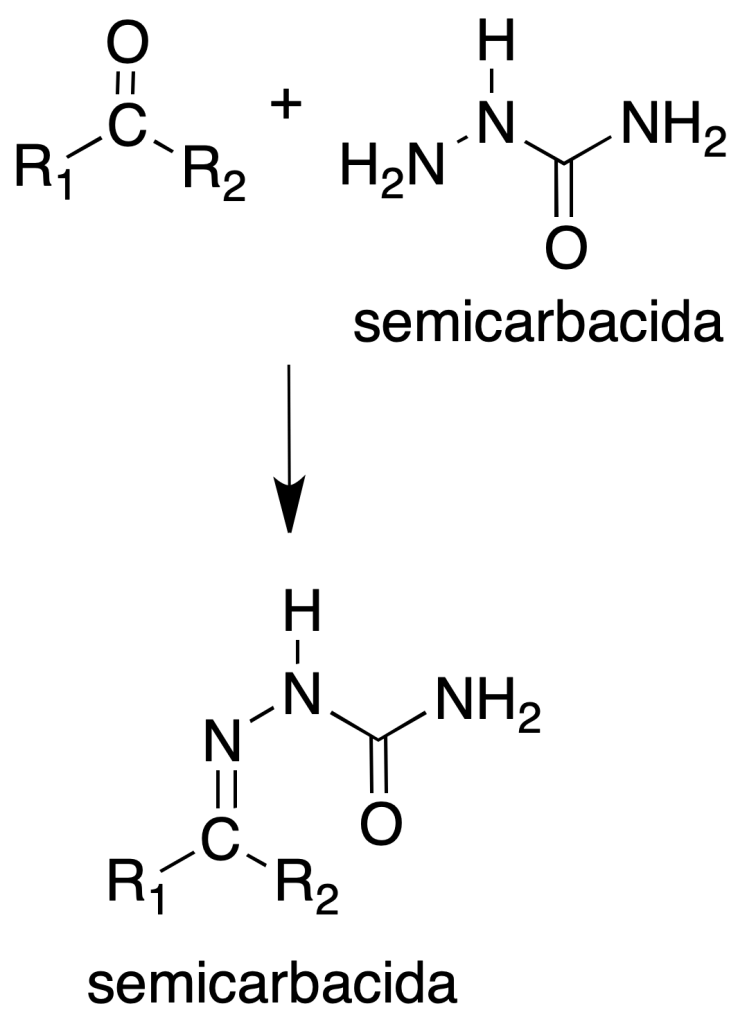
Procedimiento: En un tubo de ensayo colocar 100 mg de clorhidrato de semicarbazida, 150 mg de acetato sódico, 1 ml de agua y 1 ml de EtOH. Añadir 100 mg de compuesto carbonílico. Si la mezcla está turbia añadir más EtOH hasta hacerla clara. Agitar la mezcla durante unos minutos y dejarla reposar.
La reacción puede acelerarse calentando en un baño de vapor durante 10 min y enfriando luego en un baño de hielo. Los cristales se separan por filtración y se lavan con agua fría. Se suelen recristalizar de MeOH o EtOH, a veces con ayuda de agua.
Oximas
Pueden obtenerse como las semicarbazonas con calentamiento. Pero también como sigue:
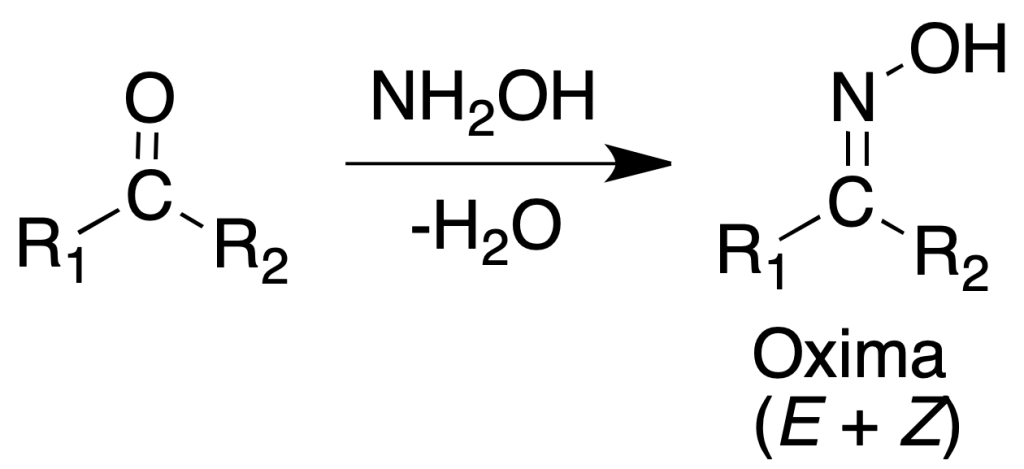
Procedimiento: Calentar a reflujo una mezcla de 100 mg de aldehído o cetona, 100 mg de clorhidrato de hidroxilamina, 2 ml de EtOH y 0.5 ml de piridina en un baño de agua durante 15 a 60 min. Eliminar el disolvente a presión reducida.
Añadir varios mililitros de agua fría y triturar a fondo. Recoger la oxima y recristalizarla de EtOH, EtOH/H2O o benceno.
Volver a la página de análisis de grupos funcionales.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.
