Written by J.A. Dobado | Last Updated on 1 año
Objetivo
Determinación de la concentración de cationes de una muestra de agua mediante el empleo de una resina sulfónica en ciclo ácido, que nos va a permitir el número total de meq/l de cationes del agua corriente.
Índice
Antecedentes
Los iones más comunes presentes en el agua potable son:
Na+, K+, Ca2+, Mg2+, HCO3–, Cl–, SO42–, H+, OH–
De forma que la suma algebraica de las cargas presentes en el agua sea 0, según el principio de electroneutralidad.
La determinación de la concentración iónica del agua corriente es una tarea importante en la industria del tratamiento del agua y en la monitorización de la calidad del agua.
Esta técnica es comúnmente utilizada en la purificación del agua y en la monitorización de la calidad del agua.
Existen varios tipos de resinas cambiadoras iónicas disponibles, cada una con una afinidad específica por ciertos iones. Por ejemplo, algunas resinas son específicas para el intercambio de iones de calcio (Ca2+) o magnesio (Mg2+), mientras que otras son específicas para el intercambio de iones de sodio (Na+) o cloruro (Cl–).
Resinas aniónicas y catiónicas
Las resinas de cambio iónico son moléculas orgánicas complejas insolubles en agua, que poseen átomos o grupos de átomos ionizables unidos a un polímero con grupos polares que pueden asociarse a cationes y aniones.
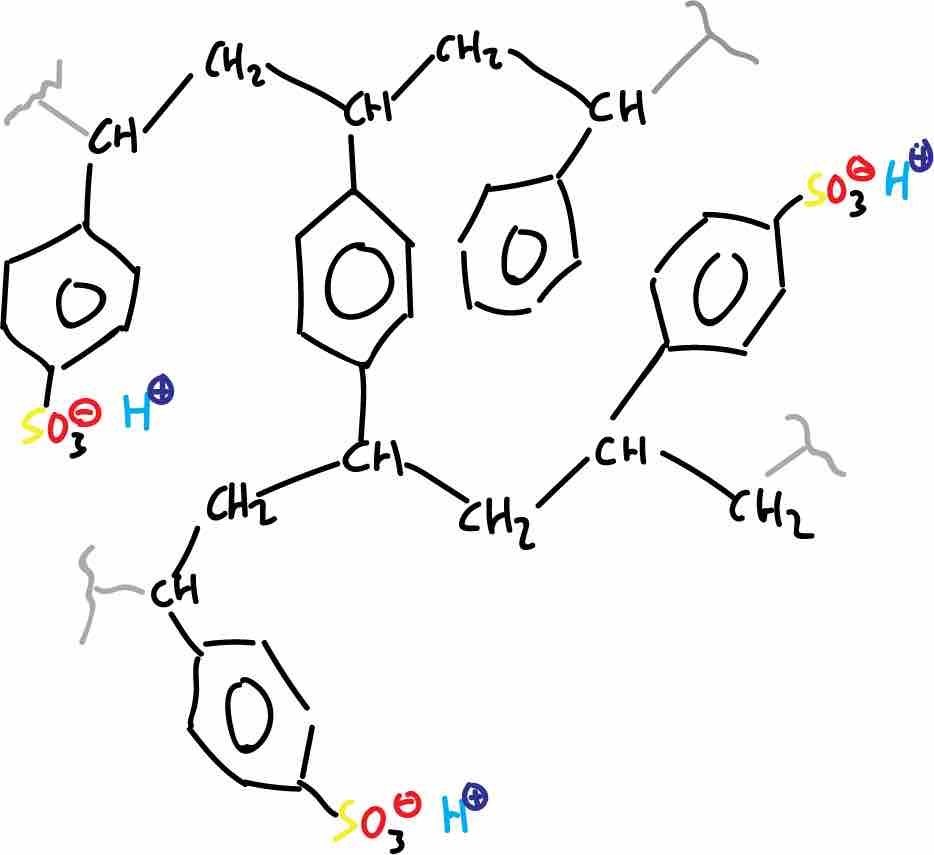
Aquellas que poseen cationes reemplazables, tales como sodio (Na+) o hidrógeno (H+) reciben el nombre de resinas catiónicas, mientras que las que poseen aniones intercambiables reciben el nombre de resinas aniónicas.
El intercambio de iones se genera mediante procesos de equilibrio.
R-SO3– H+ + M+ ↔ R-SO3– M+ + H+
Aplicaciones de las resinas cambiadoras
Las aplicaciones de las resinas cambiadoras son múltiples, destacando entre otras el tratamiento de aguas duras tanto para uso industrial como para uso doméstico.
Aunque es una técnica precisa y fiable. Sin embargo, presenta limitaciones a tener en cuenta. Por ejemplo, la resina puede saturarse después de un uso prolongado, lo que puede afectar la precisión de los resultados. Además, la técnica requiere de un cierto grado de habilidad para manejar y preparar la resina.
Procedimiento experimental
El montaje consiste en resina cambiadora iónica (volumen de resina 15 ml aproximadamente) colocada en el interior de una columna de vidrio con una base de vidrio molido en el interior para evitar que se salga y una llave. El conjunto se sujeta con una pinza.
| Es de vital importancia evitar en todo momento la formación de burbujas en su interior, y que la resina se seque a lo largo de toda la práctica, por lo que se mantendrá siempre un volumen de líquido mínimo de 1 ml por encima del lecho de sólido |
- A dicha columna se le añaden en pequeñas porciones 25 ml de disolución de HCl 2N manteniendo abierta la llave (30 gotas/min aprox).
- A continuación se lava la columna con agua desionizada (mili-Q) hasta eliminar totalmente el exceso de acidez para lo cual el eluyente debe tener pH neutro (comprobar con papel indicador).
- Medir 100 ml de agua corriente y pasarla a través de la resina a una velocidad de 30 gotas/min aproximadamente, recogiéndose sobre un matraz erlenmeyer.
- Lavar la resina con agua desionizada (15-20 ml), para arrastrar el volumen de la muestra que aún queda en la columna, recoger esta cantidad y adjuntarla a la muestra.
- Calentar la disolución hasta ebullición y dejar enfriar.
- Valorar la disolución procedente del intercambio iónico con una disolución de NaOH 0.02 N, utilizando fenolftaleína (3 gotas) como indicador.
- Determinar la concentración de bicarbonatos del agua potable tomando 100 ml de una muestra de agua del grifo y proceder a su valoración con HCl 0.02 N usando rojo de metilo (3 gotas) como indicador.
Resumen de cálculos realizados
A) Valoración del agua sometida a intercambio iónico:
Volumen de la muestra de agua…………………….
Volumen de NaOH gastado…………………………….
Contenido de cationes + HCO3– del agua………
B) Determinación del contenido de bicarbonatos
Volumen de agua tomado………………………………..
Volumen de HCl gastado…………………………………..
Contenido de HCO3– del agua……………………………
C) Contenido total de cationes del agua
C = A – B
