Written by José | Last Updated on 2 meses
¿Qué es la eliminación (E1 y E2)?
Al igual que en las reacciones de sustitución, las reacciones de eliminación siguen dos mecanismos diferenciados denominados E1 y E2.
Índice
Eliminación E1
En la reacción E1, la velocidad de reacción depende únicamente de la concentración de sustrato. El mecanismo de la reacción es similar al de la SN1, con la diferencia que el carbocatión intermedio evoluciona hacia la formación de un alqueno por pérdida de un hidrógeno en posición contigua a donde se encuentra la carga positiva.
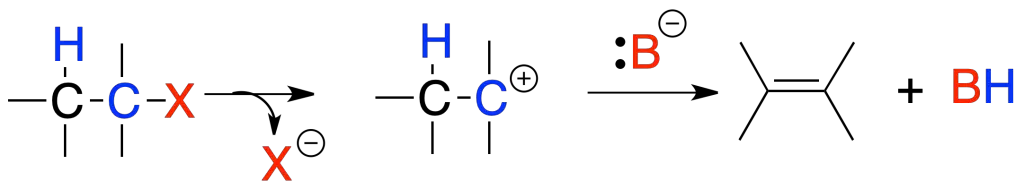
La reacción se favorece con la formación de carbocationes estables, buenos grupos salientes y bases débiles. De aquí se deduce que el orden de reactividad es terciario > secundario >>> primario. Además, se suele formar el alqueno más estable (el más sustituido) y si hay posibilidad predomina el isómero trans sobre el cis.
Eliminación E2
En la reacción E2, el tratamiento de un haluro de alquilo primario o secundario con una base fuerte conduce a la formación de un alqueno. La velocidad de reacción depende de la concentración del sustrato y de la base.
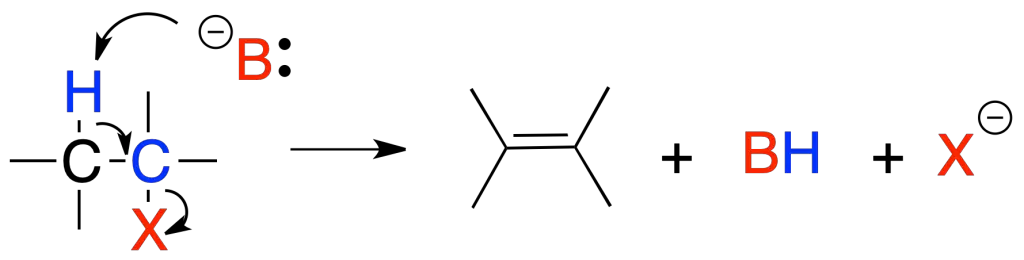
El mecanismo que se propone es un proceso concertado y los grupos que se eliminan, X y H, se disponen de forma antiperiplanar.
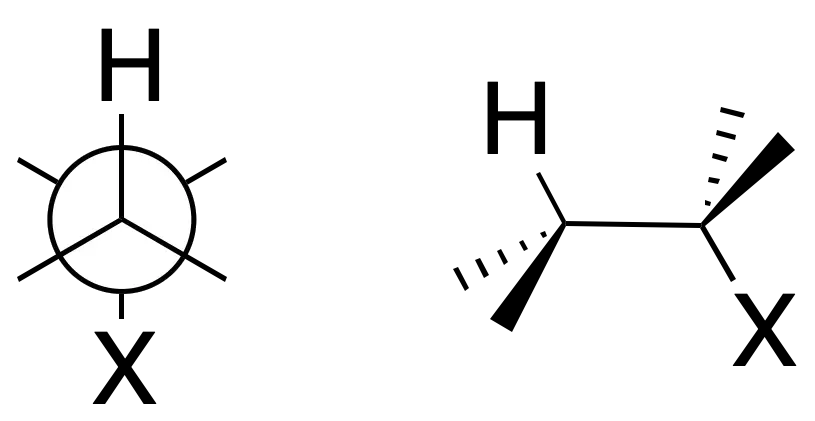
El proceso es regioselectivo, ya que en la eliminación se produce mayoritariamente el alqueno más sustituido (regla de Zaitsev). Si existe la posibilidad de formación de los isómeros cis y trans, predomina la formación del alqueno trans frente al cis.
Si se usa una base voluminosa (el caso típico es el terc-butóxido potásico), se forma mayori-tariamente el alqueno menos sustituido (regla de Hofmann), dado que prevalecen factores de tipo estérico.
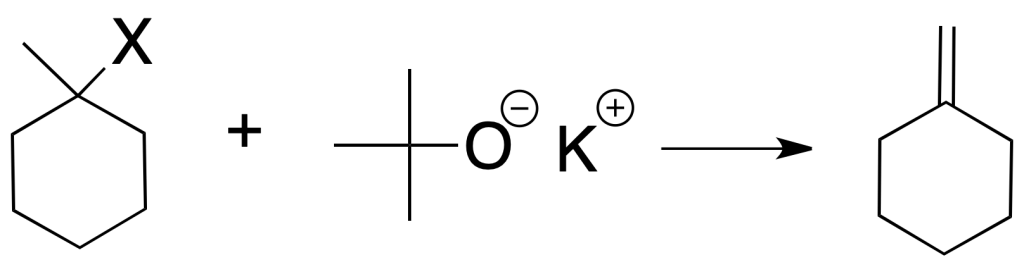
A igualdad de otros factores, la velocidad de la reacción depende de la naturaleza del halógeno, según esta secuencia I > Br > Cl >> F. La reacción es incompatible con grupos sensibles a bases.
Las reacciones de sustitución y eliminación son competitivas, y un factor importante es la temperatura. A altas temperaturas se favorece la eliminación.

