Written by José | Last Updated on 2 meses
Objetivo
Preparación de jabón mediante la reacción de un aceite vegetal con hidróxido de sodio (reacción de saponificación).
Índice
Antecedentes
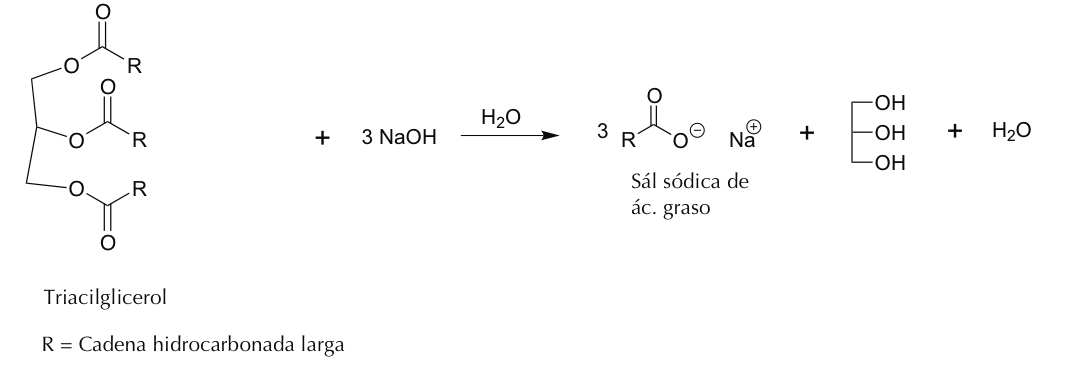
El jabón (éster metálico o carboxilato) se forma como producto de una reacción de saponificación. Se denomina reacción entre un ácido carboxílico y una base fuerte como el hidróxido de sodio NaOH o el hidróxido de potasio KOH. La característica principal es la presencia de jabón en la molécula que tiene dos zonas de diferente polaridad: una hidrofílica (o lipofóbica) y otra lipofílica (o hidrofóbica). La región hidrofílica ubicada alrededor del grupo carboxilo está fuertemente polarizada y también forma enlaces de hidrógeno con las moléculas de agua. La región lipofílica, que es muy polar, se mantiene alejada de las moléculas de agua y corresponde a la cadena hidrocarbonada. Por su carácter dual anfifílico (hidrofílico-lipofílico), las moléculas de jabón tienen la propiedad de solubilizar moléculas polares y no polares. Las moléculas de jabón muestran una fuerte tendencia a migrar a las interfases, de modo que la parte polar está dentro del agua y la parte apolar se encuentra frente a una parte apolar como el aire o el medio graso. Esta tendencia a orientar su estructura con respecto a las moléculas de agua y jabón reduce la tensión superficial en una interfase aire-agua o aceite-agua, por lo que dichas moléculas se denominan tensoactivos.
Procedimiento experimental
En un vaso de precipitados de 100 ml, disolver 9 g de NaOH en 12 a 15 ml de solución EtOH/agua (50 %). En otro vaso de 100 ml, pesar 5 g de aceite de girasol y añadir a la solución que contiene NaOH. Calentar suavemente la mezcla y agitar continuamente con una varilla de vidrio durante 15 min. Retirar el vaso de la placa caliente si se forma espuma y remover hasta que la espuma disminuya. Enfriar la mezcla y verterla, sin dejar de remover, en una solución fría de 15 g de NaCl en 60 ml de agua. A continuación, enfriar a temperatura ambiente, y luego enfriar en un baño de hielo o colocar en el congelador. Enfriar la solución para precipitar el jabón, que se aísla por filtración a vacío. Lavar el sólido resultante tres veces con agua fría, secar, pesar y calcular el rendimiento.
Propiedades físico-químicas
La siguiente tabla recoge los datos de peso molecular (Mw), punto de fusión (P.F.) punto de ebullición (P.E.) y densidad de los reactivos y compuestos utilizados en este experimento de laboratorio.
| Name | Mw (g/mol) | M.p. (ºC) | B.p. (ºC) | Density (g/ml) |
| EtOH | 46.07 | -114.1 | 78.5 | 0.790 |
| NaCl | 58.44 | 801 | 1,413 | 2.165 |
| NaOH | 40.00 | 318 | 1,390 | 2.130 |
| Aceite vegetal |
GHS pictogramas
Los pictogramas de peligro forman parte del Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos (GHS) y se recogen en la siguiente tabla para los compuestos químicos utilizados en este experimento.
| Name | GHS |
| EtOH |  |
| NaCl | No peligroso |
| NaOH |  |
| Aceite vegetal |  |
Identificador Químico Internacional
Los identificadores IUPAC InChI key de los principales compuestos utilizados en este experimento se proporcionan para facilitar la nomenclatura y formulación de los compuestos químicos y la búsqueda de información en Internet de los mismos.
| EtOH | LFQSCWFLJHTTHZ-UHFFFAOYSA-N |
| NaCl | FAPWRFPIFSIZLT-UHFFFAOYSA-M |
| NaOH | HEMHJVSKTPXQMS-UHFFFAOYSA-M |
| Aceite vegetal |

