Written by José | Last Updated on 2 meses
Objetivo
Aprender a preparar un detergente sintético, a través de la sulfonación de un anillo aromático.
Índice
Antecedentes
Los detergentes son sustancias tensoactivas, es decir, que reducen enormemente la tensión superficial del agua cuando se utilizan en concentraciones muy bajas. Los detergentes presentan una cabeza polar hidrofílica, como son las sales de ácidos carboxílicos o sulfónicos, que permite su solubilidad en el agua y una cadena carbonada que le confiere a esta parte de la molécula carácter hidrofóbico por lo que ayuda a eliminar grasas y aceites fundamentalmente de la ropa.
Para facilitar la biodegradación de estos detergentes se utilizan preferentemente cadenas hidrocarbonadas lineales en lugar de ramificadas. Los jabones se han preparado tradicionalmente mediante una reacción de saponificación de aceites de origen vegetal (ésteres de la glicerina), con lo cual se obtienen las sales sódicas de ácidos grasos.
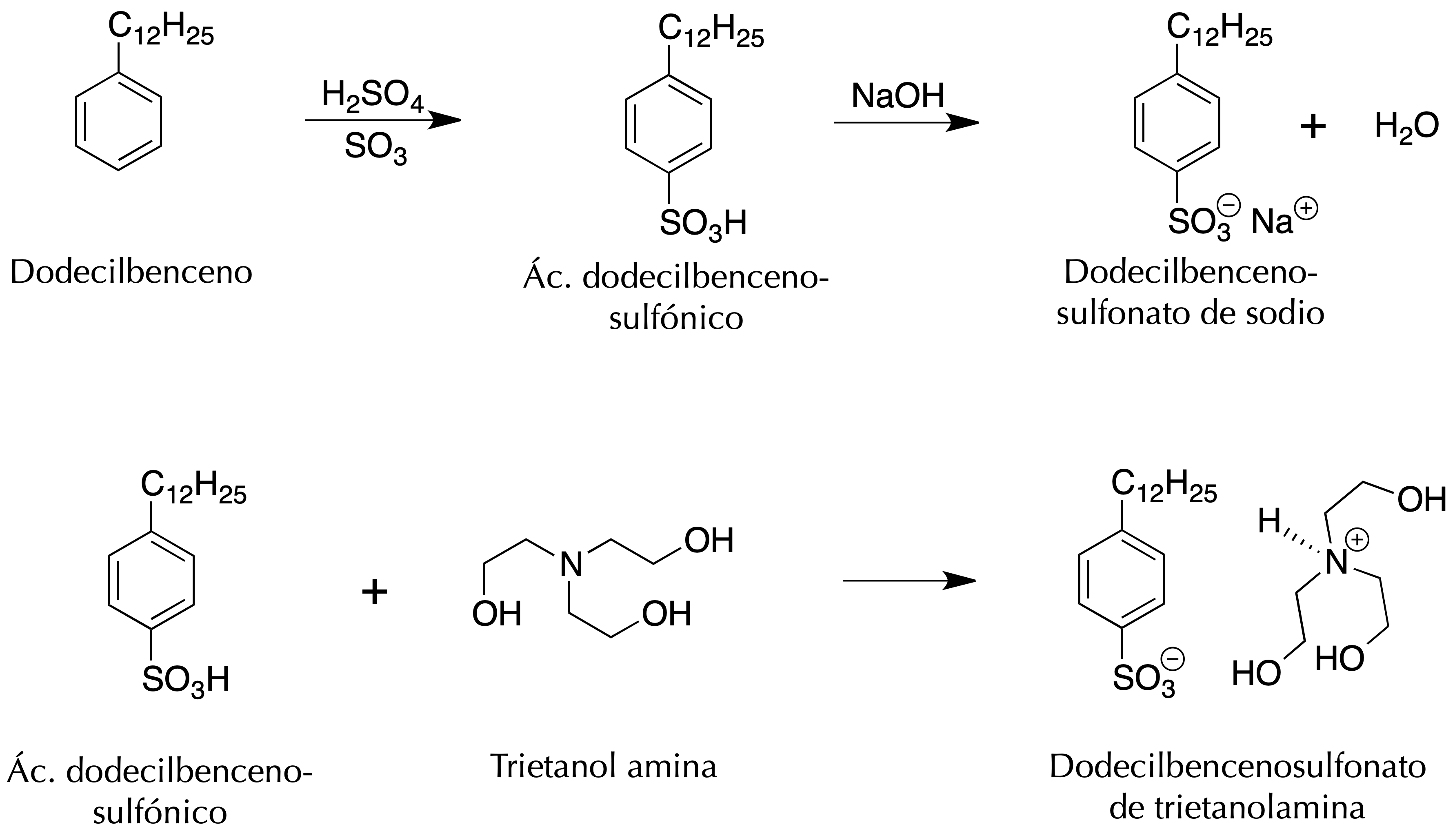
En esta práctica vamos a proceder a la preparación de un detergente líquido sintético en forma de sal amónica de la trietanolamina, a través de una reacción de sulfonación del dodecilbenceno (sustitución electrofílica aromática SEAr). Posteriormente, con el ác dodecilbencenosulfónico obtenido se procederá a la preparación de un detergente sólido mediante tratamiento con NaOH al 40 %.
Procedimiento experimental
Colocar 10 g (11.4 ml) de dodecilbenceno en un matraz Erlenmeyer de 100 ml. Añadir gota a gota durante 30 min, agitando constantemente 20 g (10 ml) de H2SO4 fumante (mucha precaución en su manejo) al dodecilbenceno, manteniendo la temperatura entre 40-45 ºC con un baño de agua/hielo. Una vez terminada la adición se calienta la mezcla de reacción en baño María a 50 ºC durante 5 min., agitando constantemente.
Enfriar la mezcla a temperatura ambiente e introducirla en un embudo de decantación hasta que se separe en dos fases. Una vez separadas, neutralizar cuidadosamente las 2/3 partes del ácido dodecilbencensulfónico obtenido, agregando gota a gota una solución de NaOH al 40 %. La parte restante neutralizarla con trietanolamina siguiendo el mismo procedimiento a fin de obtener un detergente líquido.
Propiedades físico-químicas
La siguiente tabla recoge los datos de peso molecular (Mw), punto de fusión (P.F.) punto de ebullición (P.E.) y densidad de los reactivos y compuestos utilizados en este experimento de laboratorio.
| Name | Mw (g/mol) | M.p. (ºC) | B.p. (ºC) | Density (g/ml) |
| Dodecilbencenosulfonato de sodio | 348.48 | - | - | - |
| H2SO4 | 98.08 | 3 | - | 1.80-1.84 |
| NaOH | 40.00 | 318 | 1,390 | 2.130 |
| Trietanolamina | 149.19 | 17.9-21 | 190-193 | 1.124 |
| Trietanolamina dodecilbencenosulfonato | 475.68 | - | 264 | 1.200 |
| Ácido dodecilbencenosulfónico | 326.49 | - | 82 | 1.06 |
GHS pictogramas
Los pictogramas de peligro forman parte del Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos (GHS) y se recogen en la siguiente tabla para los compuestos químicos utilizados en este experimento.
| Name | GHS |
| Dodecilbencenosulfonato de sodio |   |
| H2SO4 |  |
| NaOH |  |
| Trietanolamina | No peligroso |
| Trietanolamina dodecilbencenosulfonato |  |
| Ácido dodecilbencenosulfónico |   |
Identificador Químico Internacional
Los identificadores IUPAC InChI key de los principales compuestos utilizados en este experimento se proporcionan para facilitar la nomenclatura y formulación de los compuestos químicos y la búsqueda de información en Internet de los mismos.
| Dodecilbencenosulfonato de sodio | VQOIVBPFDDLTSX-UHFFFAOYSA-N |
| H2SO4 | QAOWNCQODCNURD-UHFFFAOYSA-N |
| NaOH | HEMHJVSKTPXQMS-UHFFFAOYSA-M |
| Trietanolamina | GSEJCLTVZPLZKY-UHFFFAOYSA-N |
| Trietanolamina dodecilbencenosulfonato | AVQBNVFOJDNROP-UHFFFAOYSA-N |
| Ácido dodecilbencenosulfónico | WBIQQQGBSDOWNP-UHFFFAOYSA-N |

