Índice
¿Qué es la prueba de Fehling?
Hermann Von Fehling descubrió en 1849 una disolución (también denominado reactivo de Fehling o licor de Fehling) que podía utilizar para la determinación de azúcares reductores. Pudiendo identificar la presencia de glucosa o sus derivados (sacarosa, fructosa, etc). Se la denomina prueba de Fehling o ensayo de Fehling.
El principio químico de esta prueba se fundamenta en la reacción de oxidación del cobre y el poder reductor de los azúcares (monosacáridos, polisacáridos, aldehídos y ciertas cetonas).
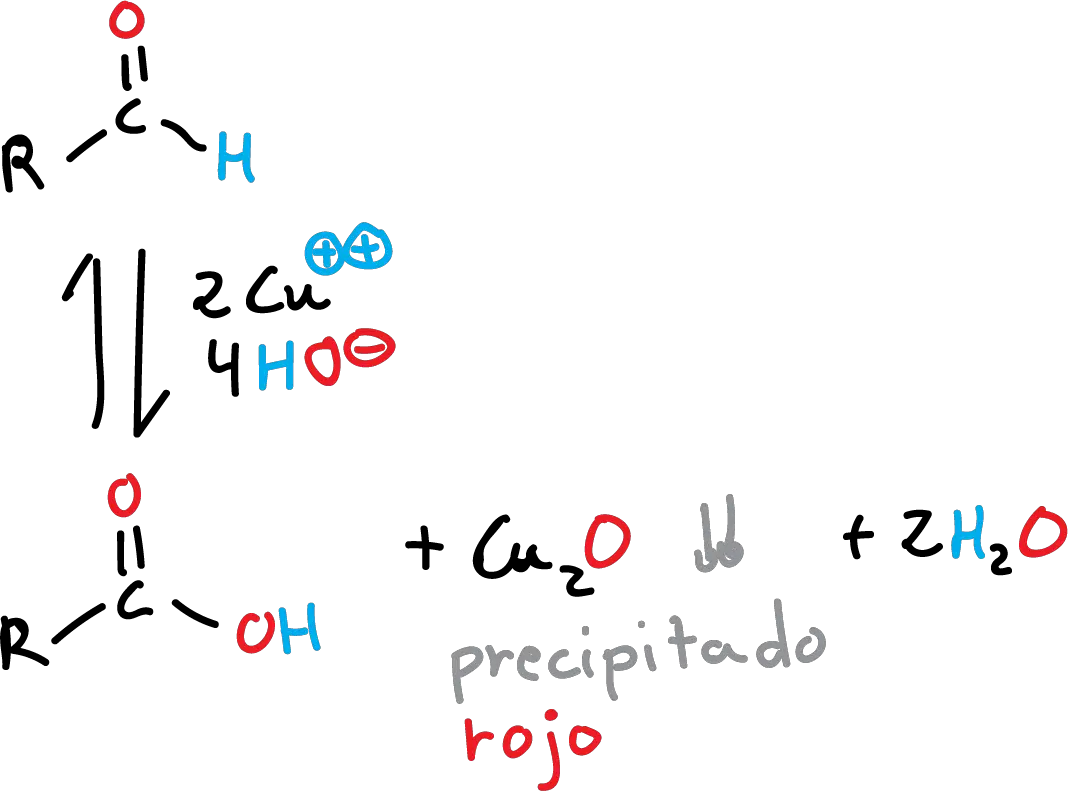
El grupo carbonilo (>C=O) de los aldehídos (tiene poder reductor) y se oxida a ácido, reduciéndose una sal de cobre a óxido de cobre. La reacción se lleva a cabo en medio alcalino y se forma un precipitado de color rojo que sirve para confirmar la presencia de dichos grupos carbonilos.
Reactivo de Fehling
Se prepara en el momento de su utilización mezclando Fehling A (disolución cúprica) con Fehling B (disolución alcalina de tartrato sódico-potásico) en partes iguales.
Se forma un complejo con el ión cúprico que es reducido por los mismos compuestos que reducían al reactivo de Tollens. Si la reacción es positiva se forma un precipitado rojo de Cu2O.
El reactivo de Fehling lo forman dos disoluciones acuosas: una de sulfato de cobre cristalizado y otra con sal seignette (tartrato mixto de potasio y sodio).
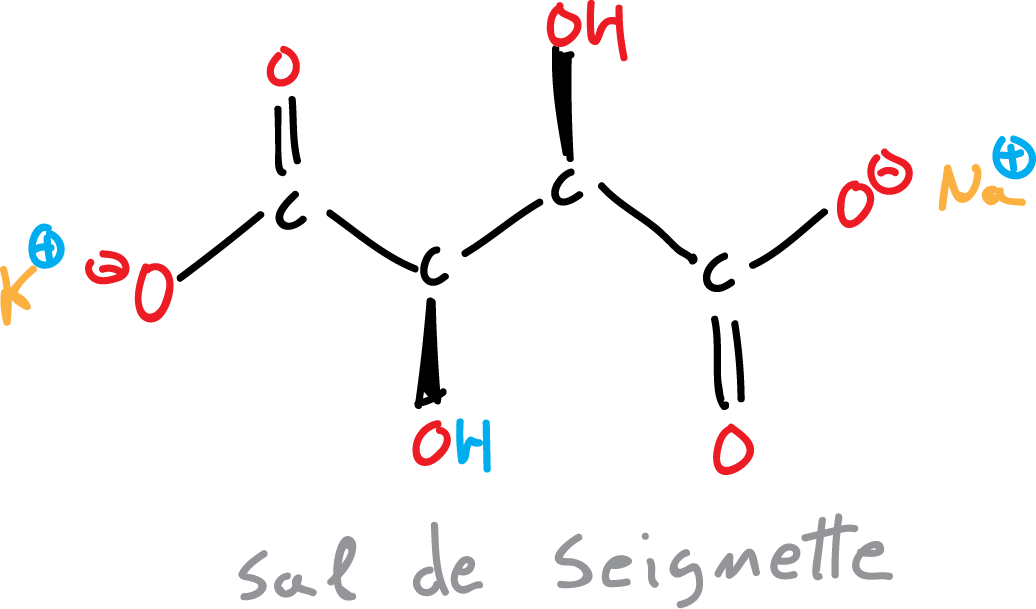
Ambas disoluciones se deben almacenar separadamente y mezclarlas sólo en el momento de su utilización.
Ejemplo de uso
Se emplea para determinar azúcares reductores, y demuestra la presencia de glucosa en la orina, y también para detectar derivados de la glucosa, disacáridos como por ejemplo: sacarosa o fructosa.
Procedimiento: Preparar dos disoluciones.
- Disolución A: Se disuelven 34.64 g de sulfato de cobre en 500 ml de agua.
- Disolución B: 17.6 g de tartrato sódico potásico y 7.7 g de NaOH disueltos en 50 ml de agua.
Cuando se requiera su utilización se mezcla 3 ml de cada una de las disoluciones. Añadir sobre esta mezcla unas gotas del compuesto líquido de la disolución del mismo y se calienta 2 min en al baño maría. Se utiliza azul de metileno para como indicador del punto final. La aparición de un precipitado rojo indica que el ensayo es positivo.
Video sobre la Prueba de Fehling
Resumen
- Ensayo positivo (+): La glucosa, lactosa y maltosa dan positivo a la prueba debido a la presencia de grupos carbonilos más expuestos que le dan carácter reductor. Se observa un precipitado rojo (óxido de cobre). La fructosa que presenta un grupo α-hidroxicetona da también un resultado positivo.
- Ensayo negativo (-): La sacarosa presenta grupos no reductores (azucar no reductor) y por tanto da resultado negativo y una coloración azul. Se puede explicar porque es un disacárido (compuesto por una molécula glucosa y otra de fructosa), los enlaces entre los dos monómeros no dejan libre ningún grupo reductor.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.
