Written by J.A. Dobado | Last Updated on 1 año
Los haloalcanos o haluros de alquilo, son compuestos derivados de los alcanos (CnHn) que presentan uno o varios grupos funcionales halogenos (F, Cl, Br, I) en la cadena carbonada.
Índice
Las reacciones más características se listan a continuación.
Reducción hasta alcanos
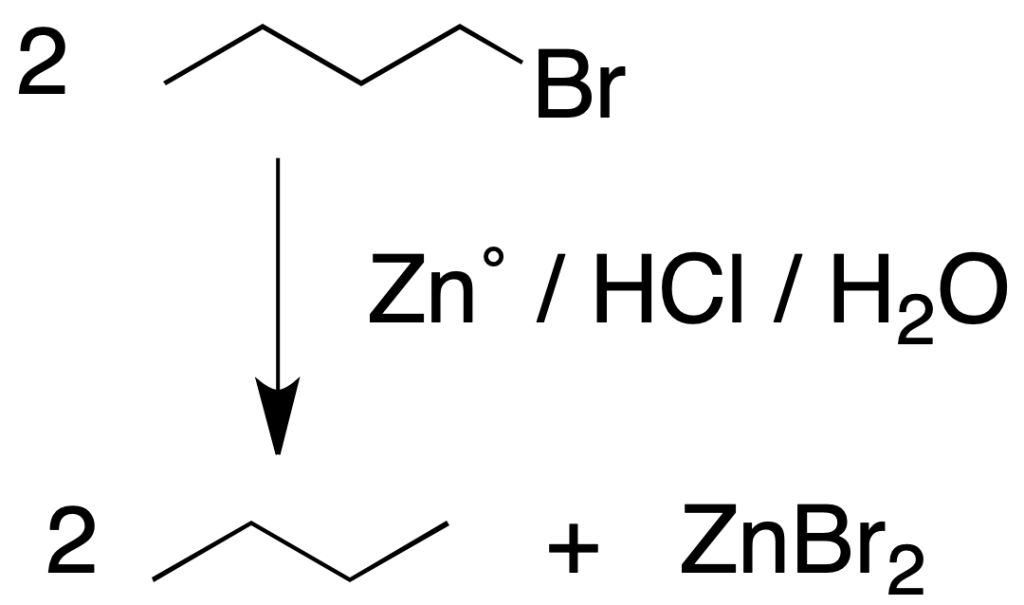
Reacción de haluros de alquilo con Zno en medio ácido
El tratamiento con Zn metálico con un ácido acuoso de un haluro de alquilo conduce a la formación de un alcano y el correspondiente haluro de zinc. Es un proceso general para la sustitución de un átomo de halógeno por hidrógeno.
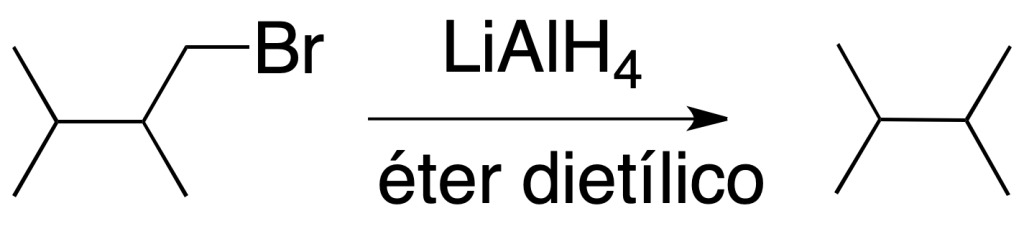
Reacción de haluros de alquilo con LiAlH4
Los haluros de alquilo primarios y secundarios reaccionan con buenos rendimientos con LiAlH4 en éter dietílico para dar alcanos. El resultado es la sustitución de un átomo de halógeno por hidrógeno.
El LiAlH4 reacciona violentamente con agua y alcoholes, siendo incompatible con una serie de grupos funcionales presentes en la molécula, por ejemplo:
| Grupo funcional | Producto final |
|---|---|
| Nitro-compuesto | Amina |
| Amida | |
| Azida | |
| Nitrilo | |
| Aldehído | Alcohol primario |
| Cloruro de acilo | |
| Ácido carboxílico | |
| Éster | |
| Cetona | Alcohol secundario |
| Epóxido | Alcohol |
| Sulfonato | Alcano |
Deshalogenación radicalaria
Los yoduros y bromuros de alquilo se reducen con buenos rendimientos hasta alcanos mediante una deshalogenación radicalaria con hidruro de tri-n-butilestaño. Los fluoruros apenas reaccionan, mientras que los cloruros lo hacen con más dificultad. El orden de reactividad para los haluros es:
terciario > secundario > primario
La reacción requiere la presencia de un iniciador de radicales como AIBN o peróxidos. Las condiciones de reacción son bastante suaves y compatibles con multitud de funciones como alquenos, compuestos carbonílicos, ácidos, lactonas, etc.).
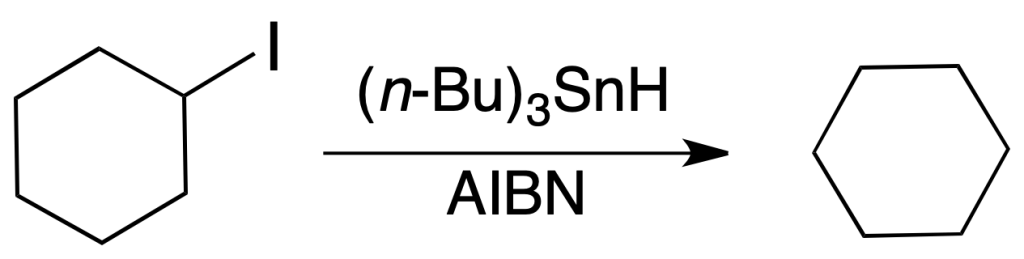
Presenta como inconveniente la toxicidad del reactivo y de los subproductos que se generan.
Deshalogenación de haluros vecinales
Debido a que los dihaluros vecinales se obtienen por adición de halógenos a alquenos, esta reacción presenta un interés relativo.
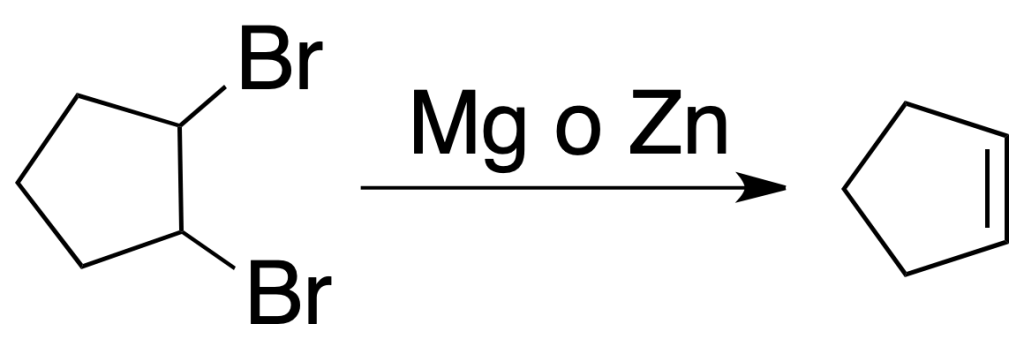
Síntesis de Wurtz (obtención de alcanos)
Consiste en la formación de un alcano a partir de dos haluros de alquilo, por tratamiento con sodio metálico. En este último caso, las mezclas de productos son muy significativas.
![]()
La síntesis de Wurtz es una de las reacciones orgánicas más antiguas y actualmente tiene interés histórico, debido a sus bajos rendimientos y a la formación de subproductos.
Síntesis de Corey-House (obtención de alcanos)
En los años 80, Corey y House desarrollaron un método, alternativo a la síntesis de Wurtz, para la síntesis de alcanos, partiendo de un haluro de alquilo, el cual reacciona con Lio. El organolítico obtenido, se trata con CuI, para dar un dialquilcuprato de litio (reactivo de Gilman), que se hace reaccionar con un haluro de alquilo.
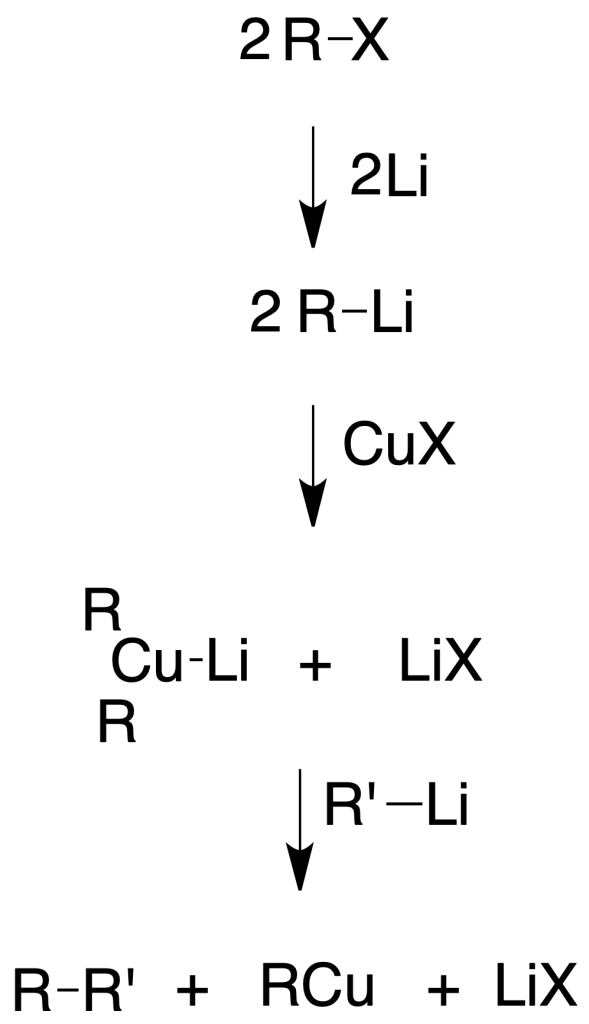
A diferencia de la síntesis de Wurtz, se ejerce un control mucho mayor sobre los productos obtenidos, evitando la formación de subproductos y se mejoran sustancialmente los rendimientos. El haluro de alquilo usado en el último paso no puede ser terciario, obteniéndose mayores rendimientos cuando éste es primario o metilo.
Sustitución nucleófila
Eliminación
Resumen de las reacciones de sustitución y eliminación
| Metilo / alquilo 1º | Alquilo 2º, 1º (o 2º estabilizado por resonancia) | Alquilo 3º | |
| SN2 | Nucleófilos fuertes | Nunca | |
| SN1 | Nunca | Nucleófilos débiles | |
| E2 | Sólo si se usan bases fuertes no nucleófilas | Cualquier base fuerte | |
| E1 | Nunca | Base débil | |
| SN2 / E2 | Haluro de metilo no da eliminación. Haluro 1º favorece SN2 | Mezclas con base nucleófila | Sólo E2 |
| SN1 / E1 | Nunca | Mezclas aunque no presente H en β | |
| Regioquímica | Estereoquímica | |
| SN2 | – | Inversión de la configuración |
| SN1 | Posibilidad de transposiciones | Mezclas racémicas |
| E2 | (regla de Zaitsev) salvo con bases voluminosas | Grupo saliente y H antiperiplanares. Se forma alqueno trans si es posible |
| E1 | (regla de Zaitsev) | Favorecido el alqueno trans |
Compuestos organometálicos
Los haluros de alquilo, arilo y vinilo reaccionan con metales para dar compuestos organometálicos. Cuando el metal es Mg, el compuesto se denomina magnesiano o reactivo de Grignard. Otros metales usados son Li, Cu o Zn. Los compuestos organometálicos son buenos nucleófilos y presentan un fuerte carácter básico.
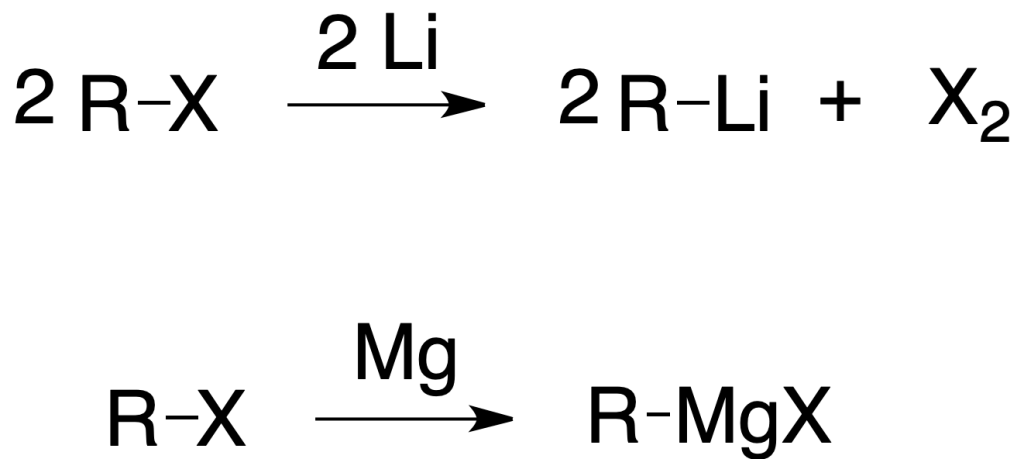
Los reactivos de Grignard sufren hidrólisis con facilidad, reduciéndose al correspondiente hidrocarburo:
![]()
o adicionarse a compuestos carbonílicos para producir, tras posterior hidrólisis, alcoholes:
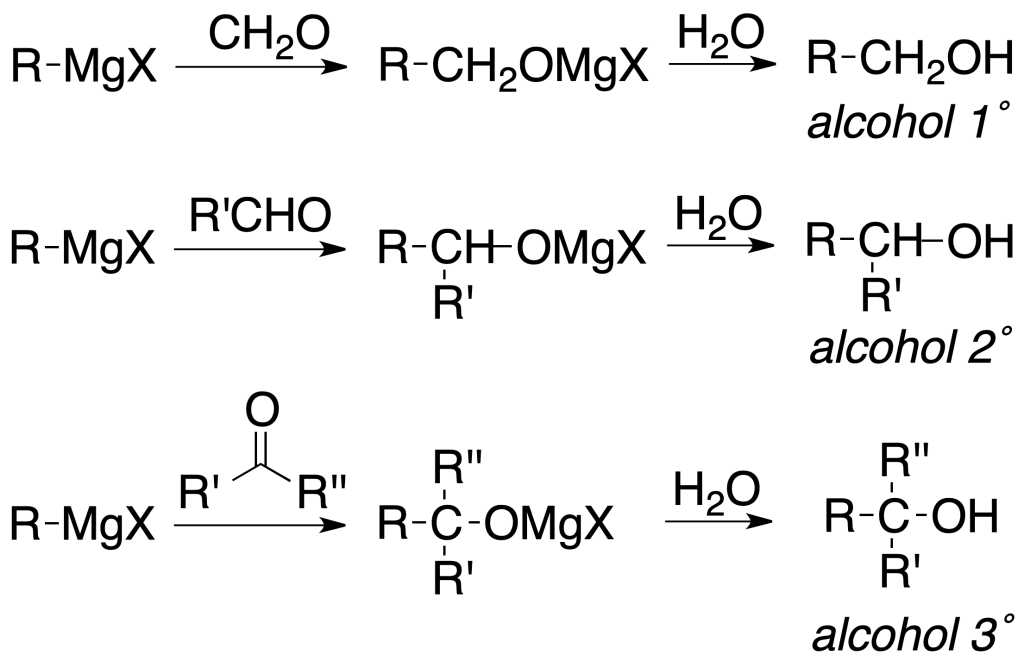
Video de Reacciones de Haloalcanos
Volver a la página de Síntesis y Reactividad de Compuestos Orgánicos.
