Written by J.A. Dobado | Last Updated on 1 año
Las reacciones de oxidación y de reducción transcurres cuando en un sustrato químico se pierde o ganan electrones, respectivamente. Y a consecuencia de esto, los grupos funcionales de la molécula se transforman hacia otros con un estado de oxidación diferente.
Índice
En este apartado, se listan las reacciones orgánicas con nombre más significativas clasificadas según el tipo de reacción química. De entre las reacciones orgánicas con nombre del tipo oxidaciones y reducciones podemos destacar las siguientes:
Condensación Aciloínica
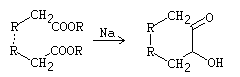
Referencias:
S.M. McElvain in Organic Reactions, Vol. 4, p. 256(New York, 1948)
Catalizador de Adkins
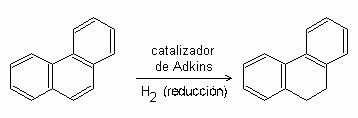
Referencias:
H. Adkins, Reactions of Hydrogen with Organic Compounds over Chromium Oxide and Nickel Catalysts, p12 (Madison, Wisconsin, 1937)
Reacción de Adkins-Peterson

Referencias:
H. Adkins, W.R. Peterson, J. Am. Chem. Soc. 53, 1512 (1931)
Reacciones de Aminoácidos de Akabori
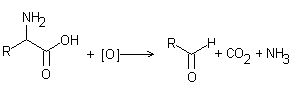
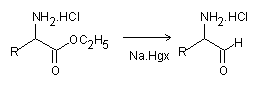
Referencias:
S. Akabori, J. Chem. Soc. Japan, 52, 606 (1931)
S. Akabori, Ber, 66, 143,151 (1933)
S. Akabori, J. Chem. Soc. Japan, 64, 608 (1943)
Oxidación de Andrussov
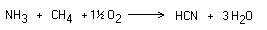
Referencias:
L. Andrussov, Ber. 60, 2005 (1927)
Reducción de Bouveault-Blanc
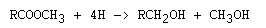
Referencias:
L. Bouveault and G. Blanc, Compt. Rend. 136, 1676 (1903)
Reacción de Cannizzaro
Reducción de Clemmensen
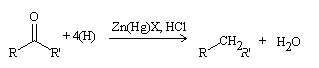
Referencias:
E. Clemmensen, Ber. 46, 1837 (1913)
E. Clemmensen, Ber. 47, 51 (1914)
E. Clemmensen, Ber. 47, 681 (1914)
Reducción de Corey-Bakshi-Shibata
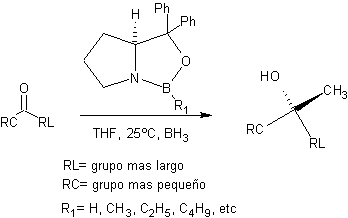
Referencias:
E. J. Corey et al., J. Am. Chem. Soc. 109, 5551 (1987)
D. J. Mathre et al., J. Org. Chem. 58, 2880 (1993)
E. J. Corey et al., J. am. Chem. Soc. 119, 11769 (1997)
Oxidación de Corey-Kim
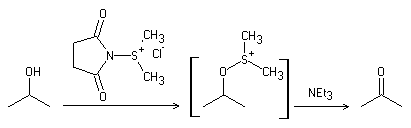
Referencias:
E. J. Corey, C. U. Kim, J. Am. Chem. Soc. 94, 7586 (1972)
E. J. Corey, C. U. Kim. Tetrahedron Letters 1974, 287
Proceso de Creighton
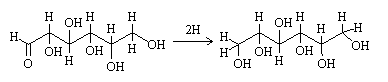
Referencias:
H.J. Creighton, U.S. patent 1612361 (1926)
H.J. Creighton, U.S. patent 1653004 (1927)
H.J. Creighton, U.S. patent 1712951 (1929)
H.J. Creighton, U.S. patent 1712952 (1929)
H.J. Creighton, U.S. patent 1990582 (1934)
H.J. Creighton, Trans. Electrochem. Soc. 75, 301 (1939)
Oxidación de Criegee
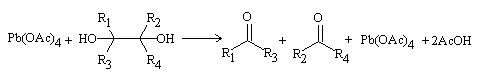
Referencias:
R. Criegee, Ber. 64, 260 (1933)
Newer Methods of Preparative Organic Chemistry, R. Criegee, vol. 1 (Interscience, New York, 1948) pp 12-20
Oxidacion de Dakin
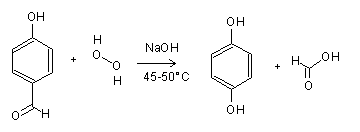
Referencias:
H.D. Dakin, J. Am. Chem. Soc. 42, 477 (1909)
Oxidación de Dess-Martin
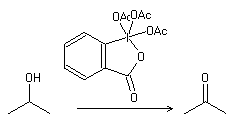
Referencias:
D.B. Dess, J.C. Martin, J. Org. Chem. 48, 4155 (1983)
R.J. Linderman, D.M. Graves, J. Org. Chem. 54, 661 (1989)
Oxidación del persulfato de Elbs
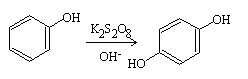
Referencias:
K. Elbs, J. Prakt. Chemie 48,179 (1893)
W. Baker, N. C. Brown and J. A. Scott, J. Chem. Soc. 1939, 1922
W. Baker and N. C. Brown, J. Chem. Soc. 1948, 2303
Reacción de Étard
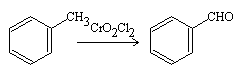
Referencias:
A.L. Etard, Compt. Rend. 90, 534 (1880);
A.L. Etard Ann. Chim. Phys. [5] 22, 218 (1881).
Reacción de Fenton
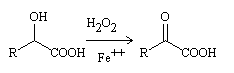
Referencias:
H.J.H. Fenton, Proc. Chem. Soc. 9, I, 113 (1893)
H.J.H. Fenton, J. Chem Soc. 65, 899 (1894); 67, 774 (1895)
H.J.H. Fenton, H. Jackson J Chem. Soc. 75, 1 (1899)
Reacción de Frankland-Duppa
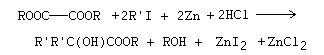
Referencias:
E. Frankland, Ann. 126, 109 (1863)
E. Frankland, B.F. Duppa Ann. 135, 25 (1865)
Reacción de Freund
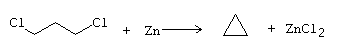
Referencias:
A. Freund, Monatsh. 3, 625 (1882)
G. Gustavson, J. Prakt. Chem. 36, 300 (1887)
H. B. Hass et al., Ind. Eng. Chem. 28, 1178 (1936).
Reacción de Guerbet
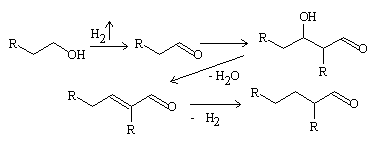
Referencias:
M. Guerbet, Compt. Rend. 128, 511 (1899)
M. Guerbet, Compt. Rend. 146, 300 (1908)
M. Guerbet, Compt. Rend. 146, 1405 (1908)
M. Guerbet, Compt. Rend. 149, 129 (1909)
M. Guerbet, Compt. Rend. 150, 183 (1910)
M. Guerbet, Compt. Rend. 154, 222 (1912)
M. Guerbet, Compt. Rend. 154, 713 (1912)
M. Guerbet, Compt. Rend. 154, 1357 (1912)
M. Guerbet, Compt. Rend. 155, 1156 (1912)
Ozonolísis de Harries
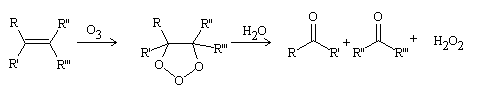
Referencias:
C. Harries, Ann. 343, 311 (1905)
H. Staudinger, Ber. 58, 1088 (1924)
L. Long, Chem. Reus. 27, 437 (1940)
Reacción de Hooker
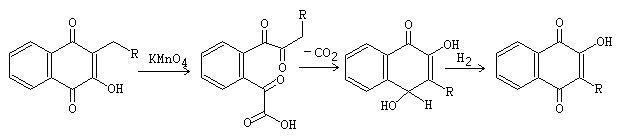
Referencias:
S.C. Hooker, J. Am. Chem. Soc. 58, 1174 (1936)
S.C. Hooker, A. Steyermark, J. Am. Chem. Soc. 58, 1179 (1936)
L.F. Fieser, M. Fieser, J. Am. Chem. Soc. 70, 3215 (1948)
L.F. Fieser, A.R. Bader, J. Am. Chem. Soc. 73, 681 (1951)
Oxidación de Jones
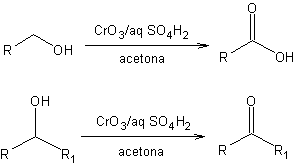
Referencias:
K. Bowden et al., J. Chem. Soc. 1946, 39
P. Bladon et al., J. Chem. Soc. 1951, 2402
E.R.AH. Jones et al., J. Chem. Soc. 1953, 457
E.R.AH. Jones et al., J. Chem. Soc. 1953, 2548
E.R.AH. Jones et al., J. Chem. Soc. 1953, 3019
Reacción de Oxidación del ácido Peryódico de Malaprade
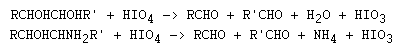
Referencias:
L. Malaprade, Bull. Soc. Chim. France 43, 683 (1928)
L. Malaprade, Compt. Rend. 186, 382 (1928)
Reacción de McMurry
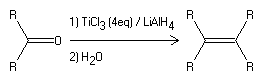
Referencias:
J.E. McMurry, M.P. Fleming, J. Am. Chem. Soc. 96, 4708 (1974)
J.E. McMurry, T. Lectka, J.G. Rico, J. Org. Chem. 54, 3748 (1989)
Reacción de Mignonac
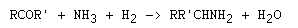
Referencias:
G. Mignonac, Compt. Rend. 172, 223 (1921)
Hidrogenación asimétrica de Noyori
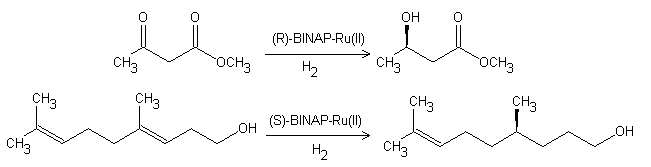
Referencias:
T. Ikariya et al. Chem. Commun. 1985, 922
R. Noyori et al., J. Am. Chem. Soc. 108, 7117 (1986)
M. Kitamura et al., Org. Syn. 71, 1 (1993)
Oxidación de Oppenauer
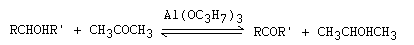
Referencias:
R. V. Oppenauer, Rec. Trav. Chirn. 56, 137 (1937).
Oxidación de Pfitzner-Moffatt
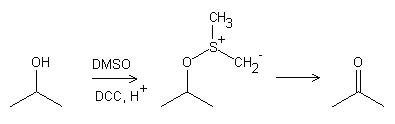
Referencias:
K. E. Pfitzner, J. G. Moffatt, J. Am. Chem. Soc. 85, 3027 (1963)
J. G. Moffatt, «Sulfoxide-Carbodiimide and Related Oxidations» in Oxidation vol. 2, R.L. Augustine, D. Trecker, Eds. (Dekker, New York 1971) pp 1-64
Reacción de Acoplamiento de Pinacol
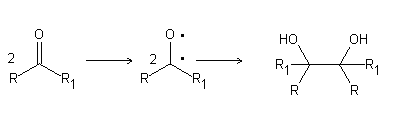
Referencias:
R. Fittig. Ann. 110, 17 (1859)
G.M. Robertson, Comp. Org. Syn. 3, 563 (1991)
Reagrupamiento de Pummerer
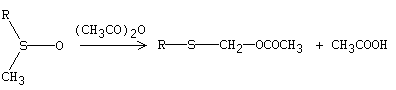
Referencias:
R. Pummerer, Ber. 43, 1401 (1910)
Horner, Kaiser, Annn. 626, 19 (1959)
Oxidación de Riley (Dióxido de Selenio)
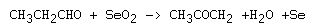
Referencias:
H. L. Riley, J. F. Morley, and N. A. C. Friend, J. Chem. Soc. 1932, 1875.
Oxidación de Rubottom
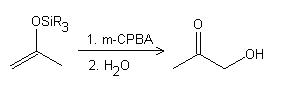
Referencias:
A.G. Brook, D.M. Macrae, J. Organometal. Chem. 77, C19 (1974)
A. Hassner et al., J. Org. Chem. 40, 3427 (1975)
G.M. Rubottom et al., Tetrahedron Letters 1974, 4319
Oxidación de Saegusa-Ito
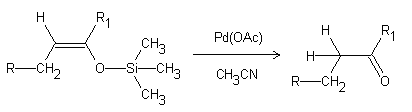
Referencias:
Y. Ito et al., J. Org. Chem. 43, 1011 (1978)
M. Kim. et al., Synth. Commun. 20, 989 (1990)
S. Porth et al., Angew. Chem. Int. Ed. 38, 2015 (1999)
Oxidación de Sarett
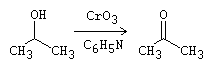
Referencias:
G.I. Poos, G. E. Arth, R. E. Beyler and L. H. Sarett, J. Am. Chem. Soc. 75, 422 (1953).
J.R. Holum, J. Org. Chem. 26, 4814 (1961)
Reacción de Staudinger
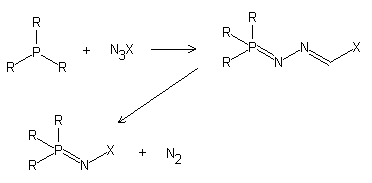
Referencias:
H. Staudinger, J. Meyer, Helv. Chim. Acta 2, 635 (1919)
Y.G. Gololobov et al, Tetrahedron 37, 437 (1981)
Oxidación de Swern
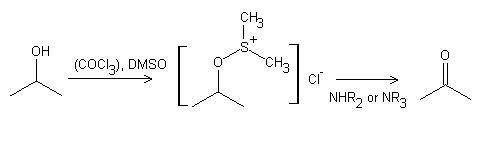
Referencias:
K. Omura, D. Swern, Tetrahedron 34, 1651 (1978)
M. Marx, T.T. Tidwell, J. Org. Chem. 49, 788 (1984)
Proceso Wacker
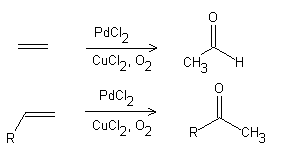
Referencias:
J. Smidt et al., Angew. Chem. Int. Ed. 1, 176 (1959)
S.X. Auclair et al., Tetrahedron Letters 33, 7739 (1992)
E. Monflier et al. Tetrahedron Letters, 36, 387 (1995)
Reacción de Willgerodt-Kindler
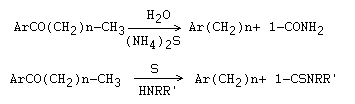
Referencias:
C. Willgerodt, Ber. 20, 2467 (1887)
C. Willgerodt, Ber. 21, 534 (1888)
K. Kindler, Ann. 431, 193 (1923)
K. Kindler, Arch. Pharm. 265, 289 (1927)
Reducción de Wolff-Kishner
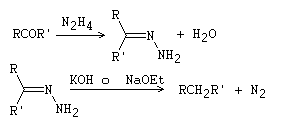
Referencias:
N. Kishner, J. Russ. Phys. Chem. Soc. 43, 582 (1911)
N. Kishner, J. Russ. Phys. Chem. Soc. 6, 347 (1912)
L. Wolff, Ann. 394, 86 (1912)
Volver a la página de Reacciones Orgánicas con Nombre y Reactivos Químicos.
