Written by J.A. Dobado | Last Updated on 1 año
¿Qué es la cloroquina?
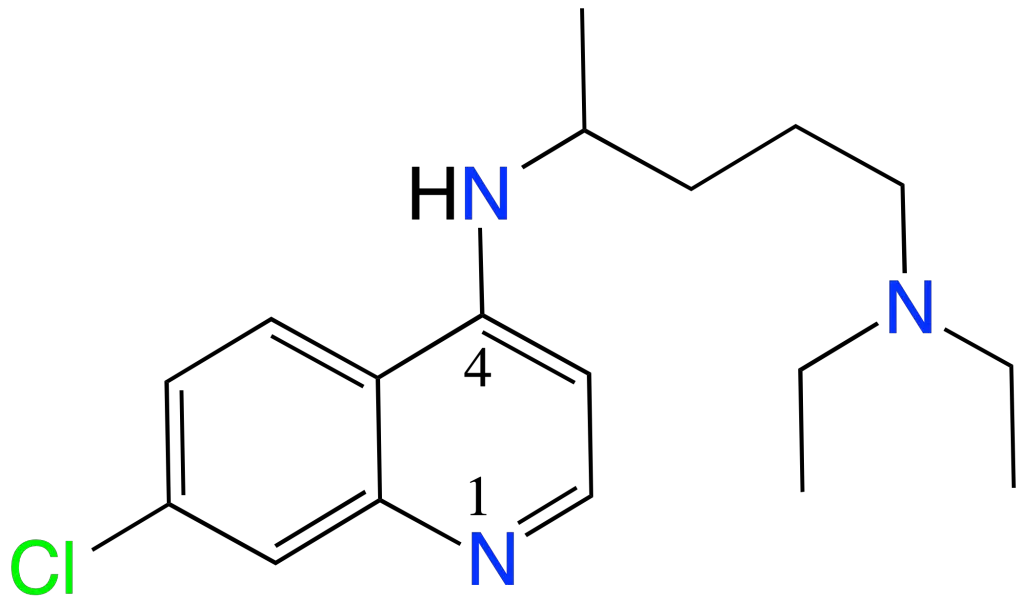
La cloroquina es una molécula de la familia de las quinolinas, en concreto de las que presentan un grupo amino (-NH2) al carbono 4 de ese anillo (4-aminoquinolinas). El nombre sistemático de la IUPAC es el (RS)-N‘-(7-cloroquinolin-4-il)-N,N-dietil-pentano-1,4-diamina.
 |
| Estructura 3D |
La aplicación principal es fármaco antiinflamatorio no esteroideo (AINE) en la prevención y tratamiento de la malaria. Igualmente, se utiliza en otras enfermedades autoinmunitarias como el lupus eritematoso sistémico y la artritis reumatoide.
La cloroquina se usaba por los indígenas del Perú, que obtenían un extracto de la corteza de los árboles Cinchona (Cinchona officinalis), se empleó como antipirético en el siglo XVII.
