Written by José | Last Updated on 2 meses
¿Qué es el naranja de metilo?
En 1865, William Perkin revolucionó las industrias de alimentos, textiles, cosméticos, papel, cuero y pinturas al preparar los primeros tintes orgánicos sintéticos. El naranja de metilo (anaranjado de metilo, heliantina, anaranjado de Poivrier, naranja gold o anaranjado III) de fórmula molecular (C14H14N3NaO3S) es una sal sódica de un diazocompuesto. El nombre sistemático de la IUPAC es 4-[[4-(dimetilamino)fenil]diazenil]benceno-1-sulfonato de sodio.
Índice
Estructura
La principal característica estructural del naranja de metilo es que presenta un grupo azo (–N=N–) unido a dos anillos aromáticos sustituidos, esta es una característica de los tintes azoicos, y representan a la clase de compuestos más utilizados en los procesos textiles y alimentarios.
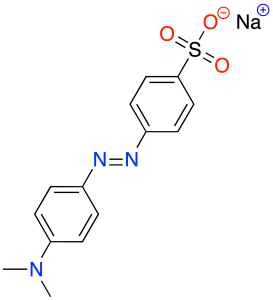 |
| Estructura 3D |
Propiedades fisicoquímicas
El estado iónico del naranja de metilo hace que este compuesto sea esencialmente no volátil. Es un sólido rojo anaranjado que no tiene olor (inodoro) y presenta las siguientes propiedades fisicoquímicas: masa molecular es de 327.34 g/mol, punto de ebullición > 300 °C, densidad de 1.28 g/cm3, siendo soluble en 500 partes de agua e insoluble en alcohol.
El naranja de metilo puede existir principalmente en dos formas diferentes, la forma alcalina (desprotonada) y la ácida (protonada). Para un pH superior a 5,5, solo hay una forma aniónica.
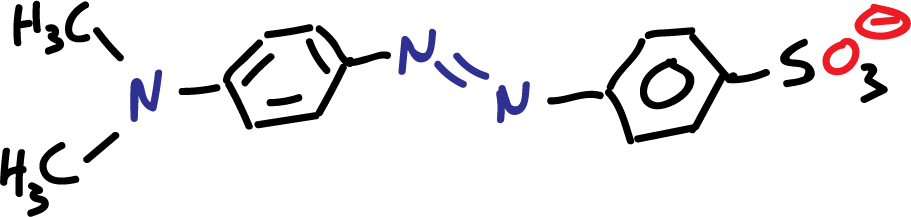
A valores más bajos de pH (ácido), una fracción de partículas cambia y para pH muy bajo (pH <2.0) solo está presente en tres especies de la forma protonada que presentan dos cargas opuestas como se indica en la figura:
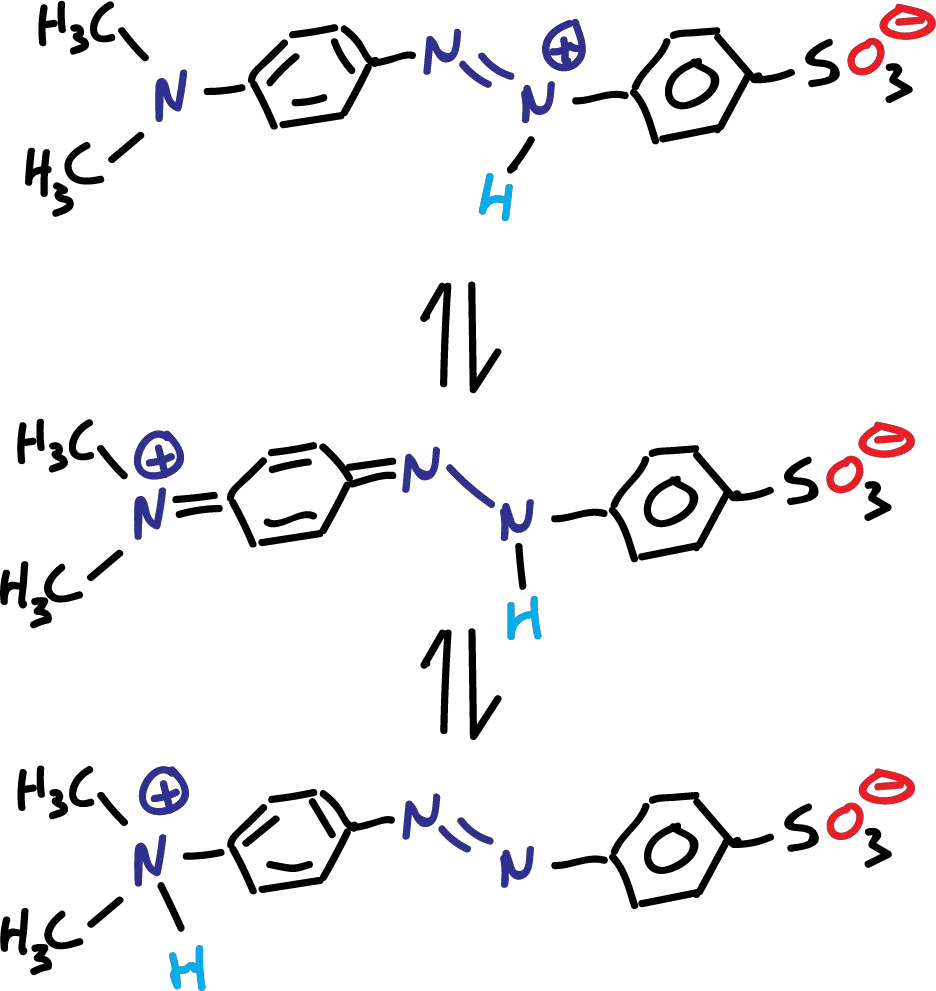
Cuando el naranja de metilo se lleva a pH ácido, los H+ se unen a un nitrógeno azocompuesto para formar un ión de azonio. Entonces, la carga positiva se distribuye al nitrógeno en el extremo de la molécula.
Aunque el grupo dimetilamino tiene una menor afinidad por H+, la formación del ion amonio también puede ocurrir a un pH bajo. Se establece un equilibrio tautomérico entre los iones amonio y azonio.
El cambio de color que experimenta el naranja de metilo, a diferente pH de debe a las distintas especies que se forman. Así como en la forma en que los electrones se reagrupan molécula cuando se une o desprende un protón (H+).
En la zona de pH (>4.4) ácida débil, neutra y básica, su coloración es amarilla naranja, y para pH (<3.1) fuertemente ácido cambia a rojo.
Usos
En 1878, se empezó a utilizar como indicador químico de pH, se emplea a una concentración de 1 gota al 0.1% por cada 10 ml de disolución. Su zona de viraje se encuentra en el rando de 3.1-4.4, y presenta un color rojo por debajo de 3,1 y amarillo anaranjado por encima de 4.4.
Hoy día se emplea ampliamente en la industria química y farmacéutica, etc. y como colorante en la industria textil, así como colorante en citología (junto con la disolución de Fuschin).
Clasificación GHS
Pictograma: Tóxico

Frase H de peligro para la salud: H301
Frase P de precaución: P264, P270, P301+P316, P321, P330, P405, P501
Perfil de reactividad
El naranja de metilo es un compuesto azoico. Los compuestos azoicos, diazoicos y azidos pueden detonar. Esto se aplica en particular a las azidas orgánicas que han sido sensibilizadas por la adición de sales metálicas o ácidos fuertes. Los gases tóxicos se forman al mezclar materiales de esta clase con ácidos, aldehídos, amidas, carbamatos, cianuros, fluoruros inorgánicos, orgánicos halogenados, isocianatos, cetonas, metales, nitruros, peróxidos, fenoles, epóxidos, haluros de acilo y agentes oxidantes o reductores fuertes. Los gases inflamables se forman al mezclar materiales de este grupo con metales alcalinos. Pueden producirse combinaciones explosivas con agentes oxidantes fuertes, sales metálicas, peróxidos y sulfuros.
Síntesis de anaranjado de metilo
Video de Naranja de Metilo
International Chemical Identifier
Se aportan los identificadores InChI key de la IUPAC para, los compuestos principales descritos en esta sección a fin de facilitar la nomenclatura y formulación de compuestos químicos y la búsqueda de información en internet de dichos compuestos.
| naranja de metilo | STZCRXQWRGQSJD-UHFFFAOYSA-M |
Referencias
- Isac-García, J.; Dobado, J. A.; Calvo-Flores, F. G.; and Martínez-García, H. (2015). Experimental Organic Chemistry Laboratory Manual. Elsevier Science & Technology. ISBN: 978-0-12-803893-2
- Vogel, A.I., Furniss, B.S., Hannaford, A.J., Tatchell, A.R., and Smith, P.W.G. (1989). Vogel’s Textbook of Practical Organic Chemistry (Vogel’s Textbook series). Longman. ISBN: 9780470214145
- Phenolphthalein and methyl orange
Charles A. Peters and Bryan C. Redmon
Journal of Chemical Education 1940 17 (11), 525
DOI: 10.1021/ed017p525

