Written by José | Last Updated on 2 meses
Síntesis de Gabriel
Se han descrito en otros apartados procedimientos sintéticos para obtener aminas, como la reducción de grupos nitro, azido y ciano o las reaciones SN2 en las que una amina actuaba como nucleófilo.
Índice
La síntesis de Gabriel es un método de obtención de aminas, principalmente primarias, en dos pasos, a partir de haluros de alquilo y utilizando ftalimida potásica, que se convierte en un primer paso en la amida terciaria cíclica (reacción SN2).
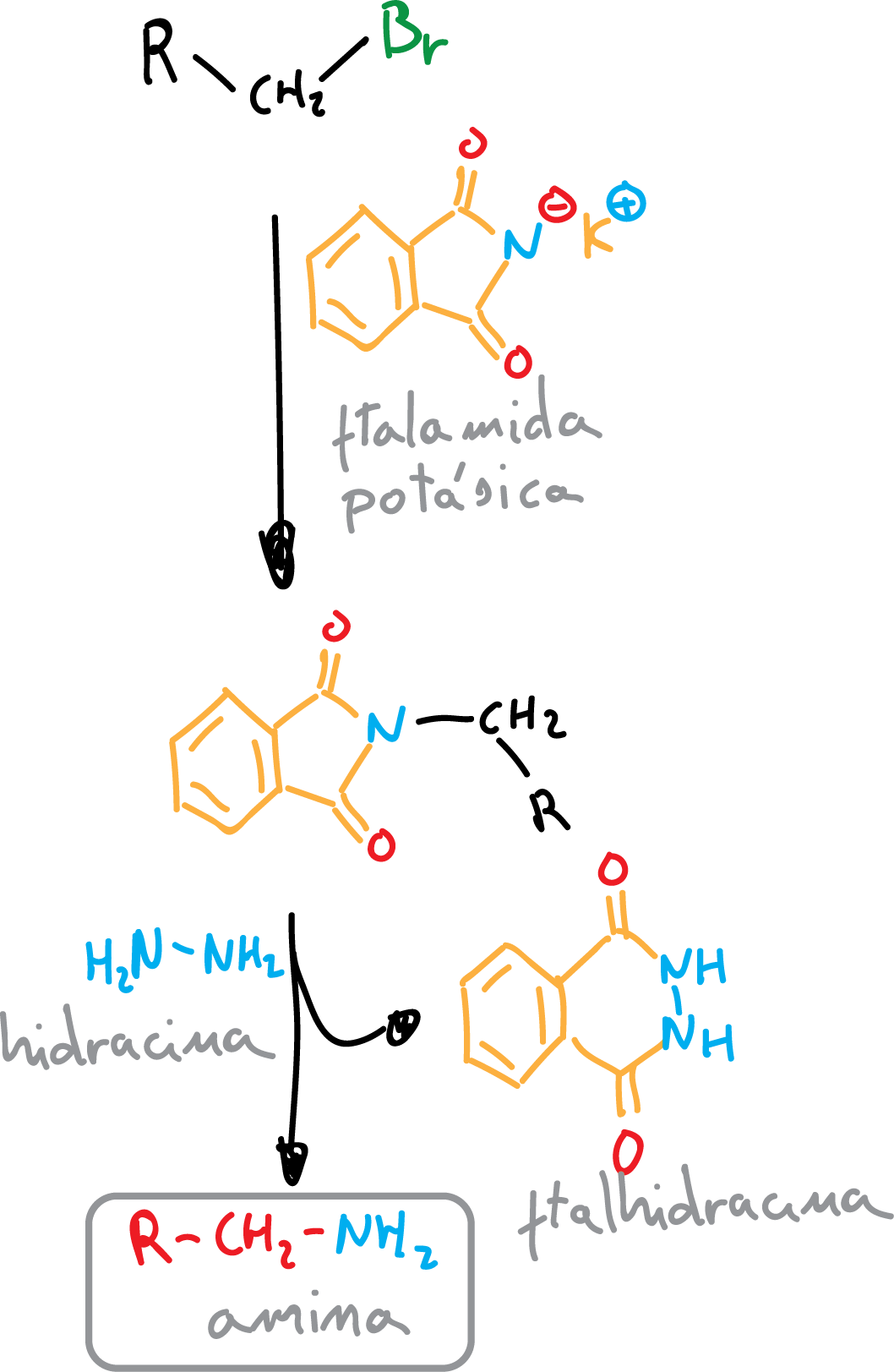
Por posterior reacción con hidrazina da como subproducto la ftalhidrazida y una amina según el haluro de alquilo de partida. Debido a que el primer paso de la reacción es una SN2, reaccionan mejor los haluros primarios sin impedimento estérico.
Alquilación
Las aminas, gracias a su par de electrones sin compartir, pueden reaccionar con electrófilos como los haloalcanos (RX). El amoníaco reacciona con 1 mol de RX para dar aminas primarias.
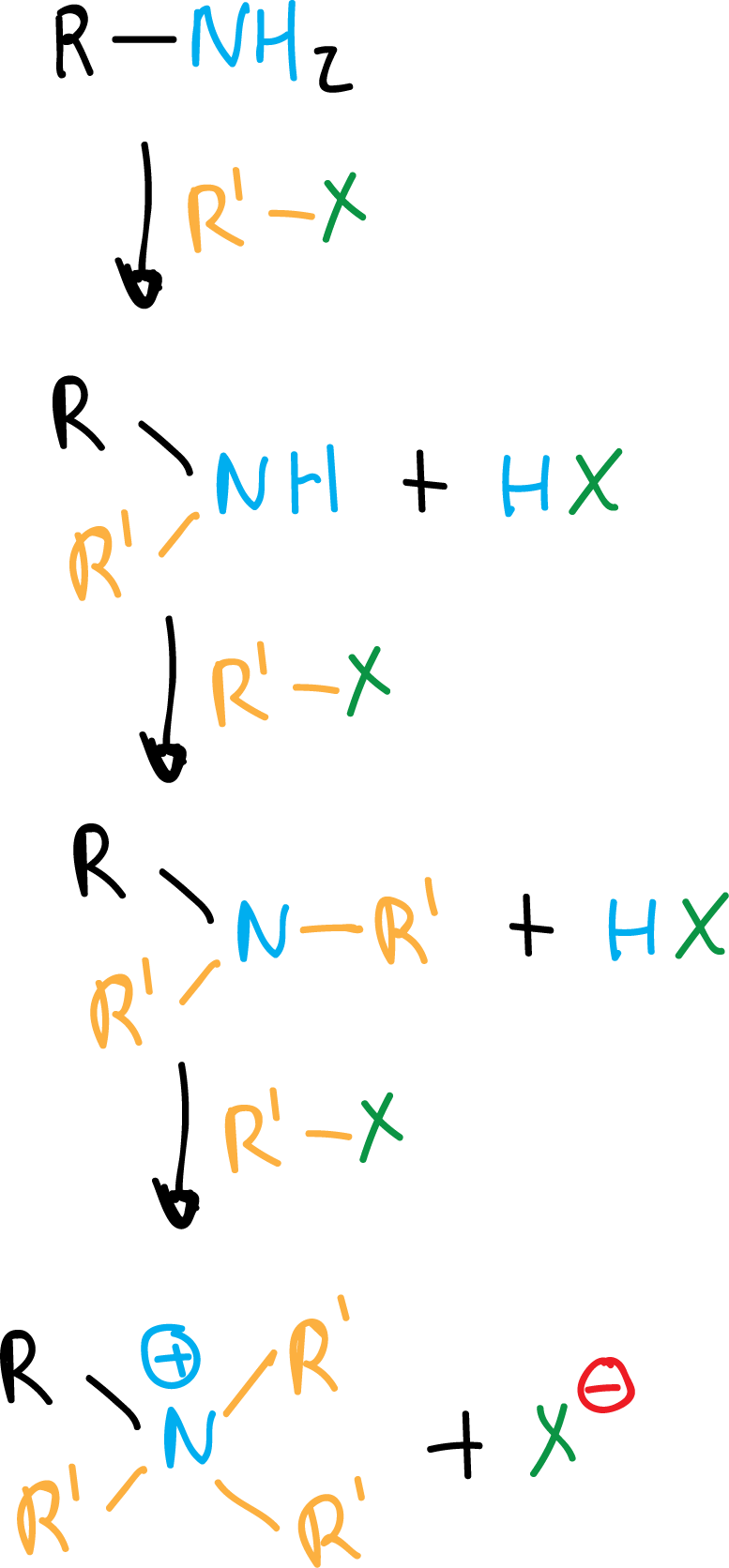
Si hay exceso de agente alquilante, vuelven a reaccionar y se convierten en aminas secundarias, y estas últimas también se transforman en aminas terciarias, y finalmente, en sales de amonio cuaternarias.
Eliminación de Hofmann
Con un exceso de RX en la reacción de alquilación se puede transformar cualquier tipo de amina en sal de amonio cuaternario. Estas sales, en medio básico, sufren la eliminación de Hofmann para dar un alqueno (el menos sustituido) y amina terciaria.
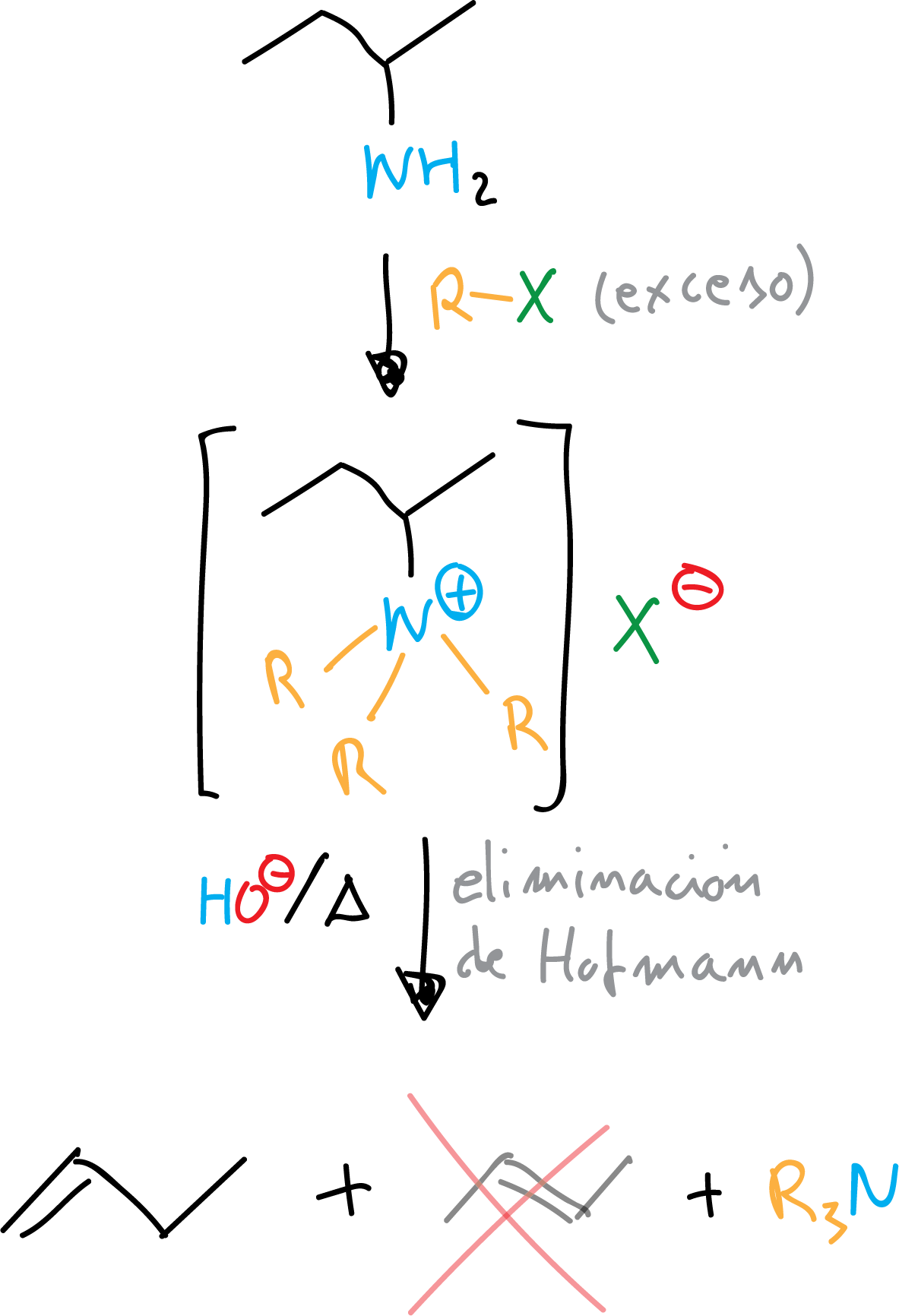
Conversión a amidas y sulfonamidas
Otros de los electrófilos que reaccionan con las aminas son los cloruros de acilo y cloruros de ácidos sulfónicos para dar amidas y sulfonamidas, respectivamente.
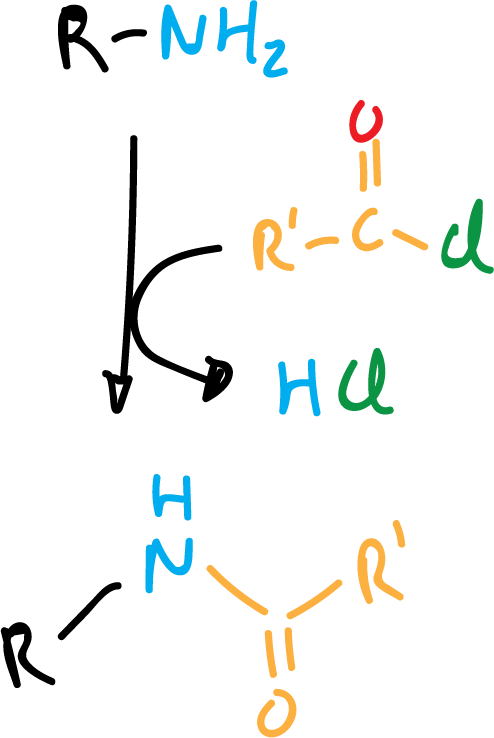
Con aminas secundarias la reacción queda como se indica en el siguiente esquema:
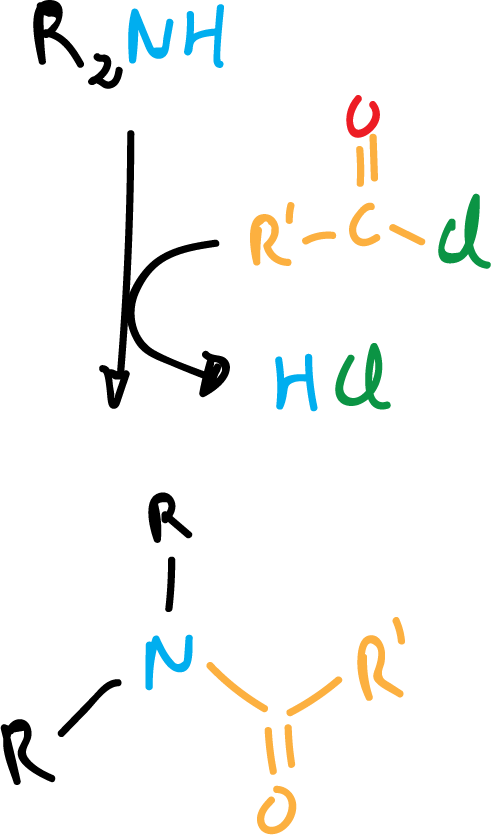
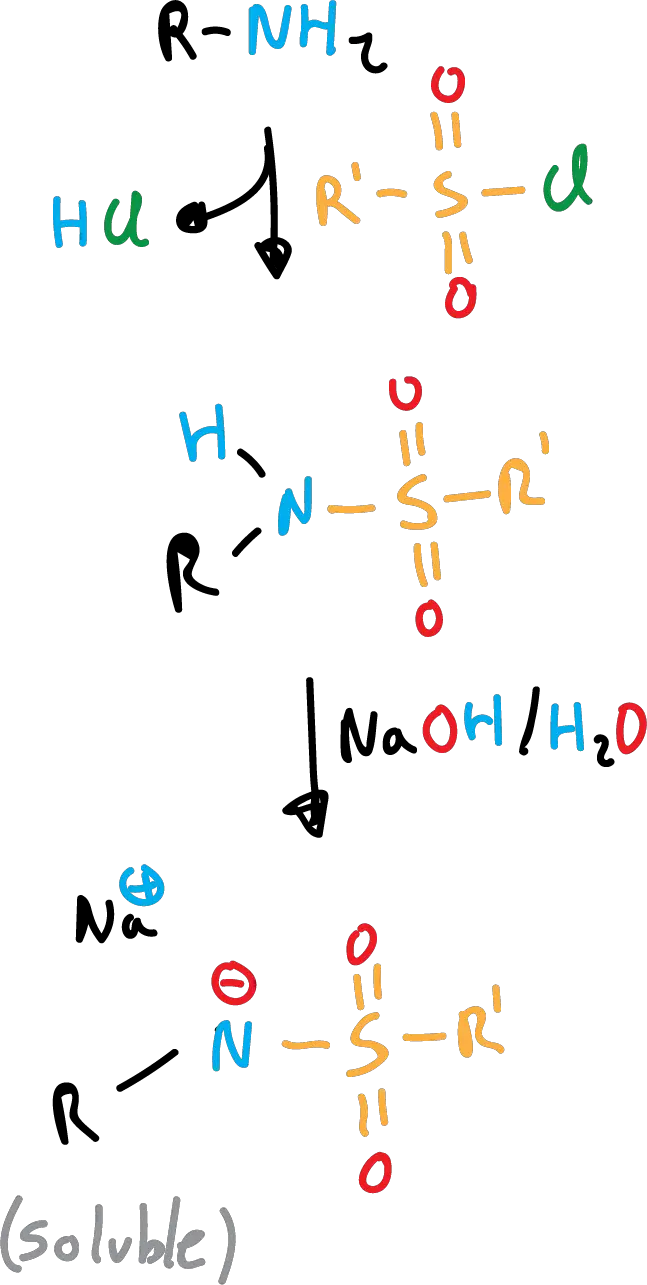
El ensayo de Hinsberg para identificar aminas primarias y secundarias se basa en la diferente solubilidad en medio básico de las sulfonamidas
Las sulfonamidas primarias son solubles debido a que se forma el anión (pérdida del protón del nitrógeno).
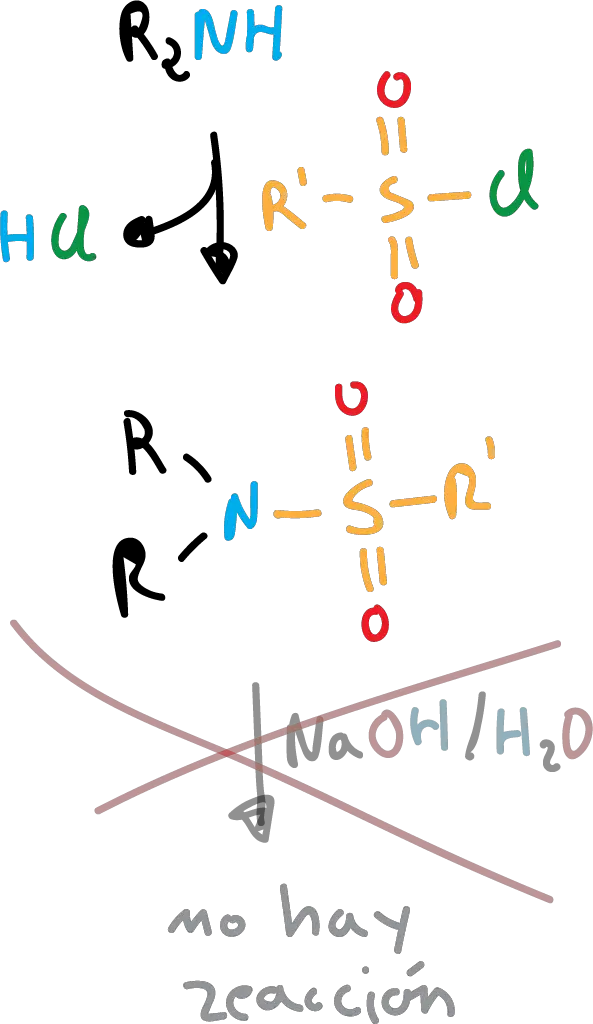
Sin embargo, las aminas secundarias al no poseer el protón son insolubles. Las aminas terciarias no reaccionan a sulfonamidas.
Reacciones con ácido nitroso
El ácido nitroso (HNO2) es otro nucleófilo que reacciona con aminas alifáticas primarias para dar sales de diazonio que posteriormente, se transforman en mezcla de alcoholes y alquenos.
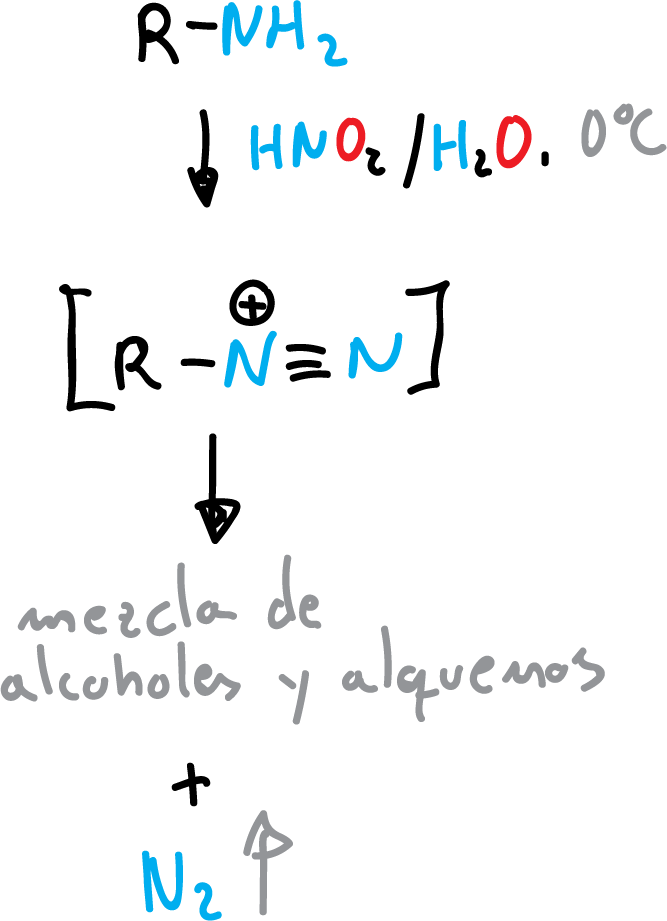
También reacciona con aminas secundarias para dar N-nitrosamina.
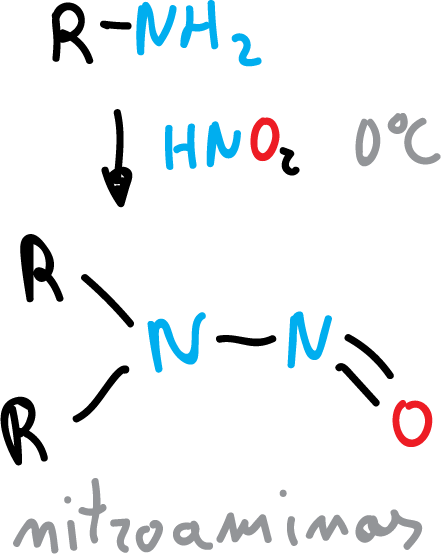
El ácido nitroso se prepara a partir del nitrito sódico (NaNO2) y HX.
Reacción de Mannich
Aunque es una reacción de condensación (véase reacciones de enoles y enolatos), y utiliza formaldehído (véase reacciones de aldehídos y cetonas) para alargar en un metileno la cadena carbonada del producto, se abordará aquí, ya que utiliza y permite obtener aminas alifáticas.
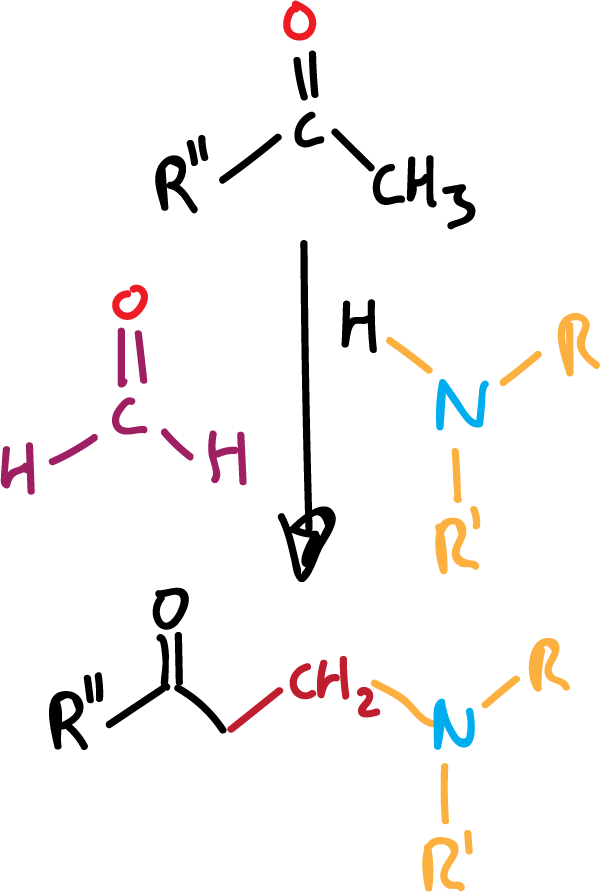
Sin duda, es una reacción versátil de conversión de aminas sencillas en otras más complejas. Se utilizan tres reactivos, un compuesto carbonílico enolizable, el formaldehído y una amina, y nos da el producto de condensación de los tres, como se indica en el esquema general de reactividad.
Volver a la página de Síntesis y Reactividad de Compuestos Orgánicos.

