Índice
Objetivo
Aprender cómo se pueden aislar diferentes compuestos orgánicos de acuerdo con sus propiedades ácido-base, que cambian su solubilidad en los disolventes orgánicos y acuosos, mediante la técnica de extracción líquido-líquido.
 |  |
 |  |
Antecedentes
La extracción líquido-líquido es una de las operaciones básicas más comunes en el laboratorio de Química Orgánica, ya que muchas reacciones implican el uso de esta técnica para el aislamiento de los productos. Los ácidos carboxílicos pueden reaccionar con bases como el hidróxido de sodio, produciendo un protón y formando los correspondientes aniones (carboxilatos) solubles en agua. Este experimento implica la separación de los componentes de una mezcla que consiste en naftaleno y ácido benzoico, que se disolverá en un solvente orgánico como CH2Cl2, dependiendo del carácter ácido o básico de dichos compuestos.
Procedimiento
Separación de dos componentes (mezcla de un compuesto ácido y neutro): Tome 30 ml de una solución problema que contiene un disolvente orgánico (CH2Cl2) y dos compuestos diferentes disueltos con carácter neutro y ácido, como son: naftaleno, y ácido benzoico, respectivamente.
Coloque los 30 ml de la disolución problema en un embudo de decantación de 250 ml. Agregue 40 ml de una disolución de NaOH al 5% y agite vigorosamente (o bien con 20 ml dos veces). Deje reposar y luego separe las dos capas (la capa acuosa es la superior y la capa orgánica, CH2Cl2, la inferior).
La capa orgánica 1-O (inferior) se seca con Na2SO4 anhidro durante unos minutos. Eliminar el desecante por filtración por gravedad. Transfiera el filtrado a un matraz de fondo redondo seco, y evapore el disolvente hasta sequedad en el rotavapor. Se obtiene el componente neutro de la mezcla como un sólido de olor característico, naftaleno.
La capa acuosa 1-A, se vuelve ácida (usar papel indicador) agregando pequeñas porciones de HCl (conc.). Enfríe la mezcla y filtre a vacío (Kitasato y Büchner), el producto cristalino obtenido es el componente ácido de la mezcla problema, ácido benzoico.
Esquema general de la separación
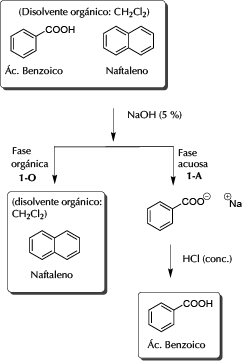
Propiedades fisico-químicas
La siguiente tabla recoge los datos de peso molecular (Mw), punto de fusión (P.F.) punto de ebullición (P.E.) y densidad de los reactivos y compuestos utilizados en este experimento de laboratorio.
| Name | Mw (g/mol) | M.p. (ºC) | B.p. (ºC) | Density (g/ml) |
| Ácido benzoico | 122.12 | 125 | 249 | 1.08 |
| Naftaleno | 128.17 | 79.5-81.0 | 218 | - |
| CH2Cl2 | 84.93 | -97 | 40.0 | 1.33 |
| NaOH | 40.00 | 318 | 1,390 | 2.130 |
| HCl | 36.46 | -30 | >100 | 1.200 |
| Na2SO4 | 142.04 | 884 | - | 2.630 |
GHS pictogramas
Los pictogramas de peligro forman parte del Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos (GHS) y se recogen en la siguiente tabla para los compuestos químicos utilizados en este experimento.
| Name | GHS |
| Ácido benzoico |   |
| Naftaleno |    |
| CH2Cl2 |  |
| NaOH |  |
| HCl |   |
| Na2SO4 | No peligroso |
Identificador Químico Internacional
Los identificadores IUPAC InChI key de los principales compuestos utilizados en este experimento se proporcionan para facilitar la nomenclatura y formulación de los compuestos químicos y la búsqueda de información en Internet de los mismos.
| Ácido benzoico | WPYMKLBDIGXBTP-UHFFFAOYSA-N |
| Naftaleno | UFWIBTONFRDIAS-UHFFFAOYSA-N |
| CH2Cl2 | YMWUJEATGCHHMB-UHFFFAOYSA-N |
| NaOH | HEMHJVSKTPXQMS-UHFFFAOYSA-M |
| HCl | VEXZGXHMUGYJMC-UHFFFAOYSA-N |
| Na2SO4 | PMZURENOXWZQFD-UHFFFAOYSA-L |
Volver a la página de prácticas de Separación de los Componentes de una Mezcla.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.
