Índice
Objetivo
Con la realización de la síntesis de p-nitroanilina, se pretende familiarizar al alumno con el concepto de grupo protector. En esta práctica de laboratorio se realizarán reacciones de protección/desprotección de un grupo amino.
De esta manera, se utilizarán reacciones como la nitración, que requieren unas condiciones fuertemente ácidas y a las que un grupo amino es sensible.
Antecedentes
La anilina no se puede nitrar de forma directa, ya que el grupo amino es muy sensible a las condiciones ácidas de la nitración.
Por tanto, se procederá en primer lugar a la protección del grupo amino, seguidamente se realizará la reacción de nitración y finalmente se eliminará el grupo protector, con lo que obtendremos el producto deseado.
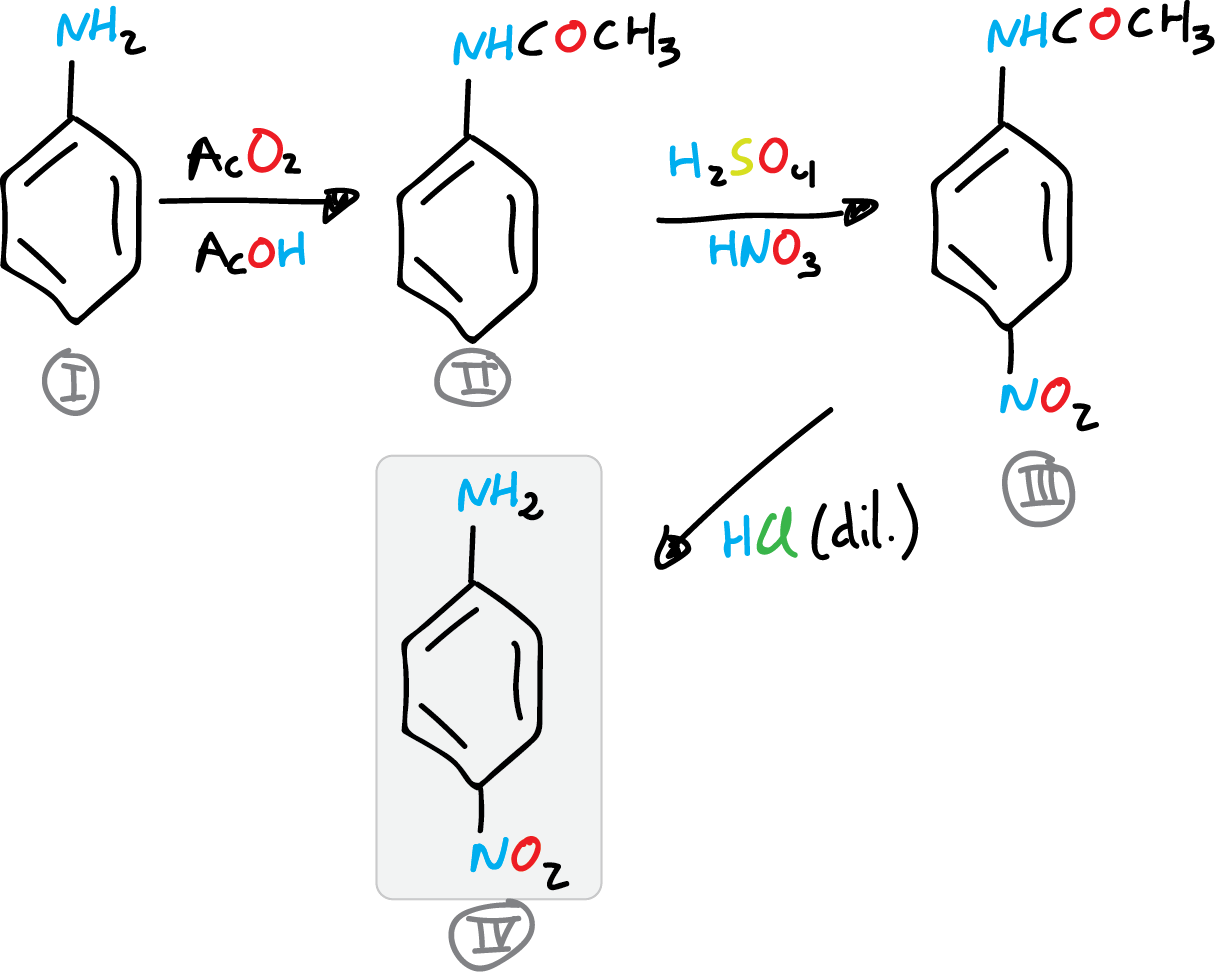
Se deberá usar en cada paso el producto obtenido en la etapa anterior, por lo que se deberá ajustar las cantidades que se indican en el procedimiento con las que se obtengan en cada etapa.
Procedimiento experimental
La síntesis de la p-nitroanilina se abordará en tres pasos, primero se obtiene la acetanilida, luego se nitra hasta p-nitroacetanilida, y por último se procede a la desprotección para dar la p-nitroanilina.
A) Preparación de la acetanilida
En un matraz de 250 ml se colocan 9 ml (0.1 mol) de anilina, 15 ml de ácido acético glacial y 15 ml de anhídrido acético. Se adapta al matraz de fondo redondo un refrigerante de reflujo, y la disolución se calienta a ebullición durante 10 min. A continuación, se deja enfríar el matraz.
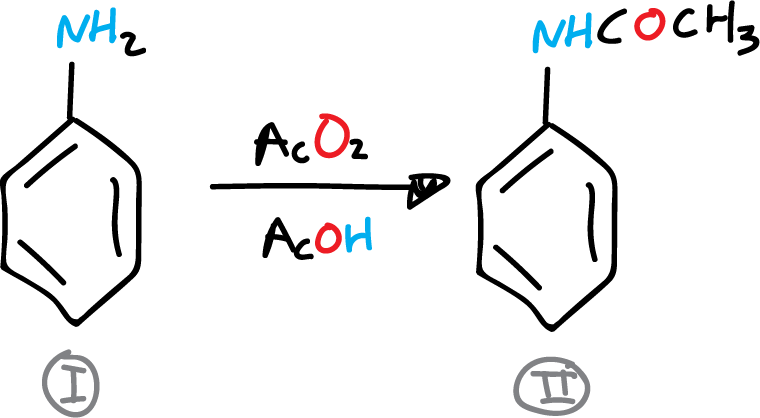
Se vierte el crudo de reacción en un vaso de precipitados con 50 ml de agua y 40-50 g de hielo. Se agita la mezcla bien y los cristales de acetanilida se recogen por filtración en un Büchner. El producto se recristaliza en agua, aprox. 200 ml, y se decolora con carbón activo. Se seca, se pesa y se determina el rendimiento.
B) Nitración de la acetanilida
En un vaso de precipitados de 100 ml se colocan 15 ml de H2SO4 concentrado y se añaden 6.75 g (0.05 mol) de acetanilida, en pequeñas porciones y con agitación magnética. Tan pronto como toda la acetanilida, o prácticamente toda, se haya disuelto, se introduce el vaso en un baño de hielo y se añade, mediante un embudo de adición, una disolución de 6 ml de HNO3 en 6 ml de H2SO4 (conc.). La mezcla se añade gota a gota, agitando suavemente y regulando la adición de modo que la temperatura de la mezcla de reacción no supere los 35 ºC.
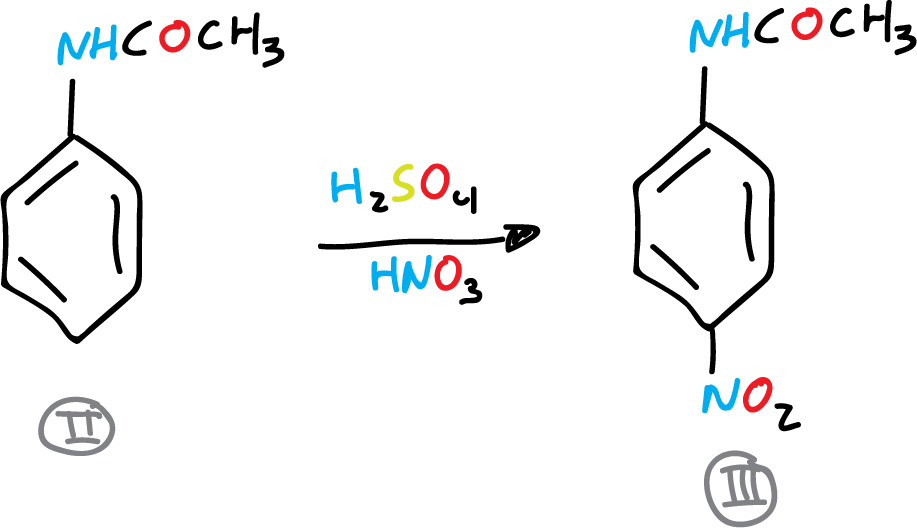
Concluida la adición, se saca el vaso del baño de hielo y se deja permanecer a temperatura ambiente durante 5 min. La solución de acetanilida nitrada se vierte sobre un vaso de precipitados de 600 ml (con aprox. 100 ml de agua y 30 g de hielo).
La mezcla se agita y el precipitado de p-nitroacetanilida se recoge por filtración a vacío en un Büchner. En el mismo Büchner se lava con dos porciones de 50 ml de agua fría prensando bien, dejando pasar una corriente de aire para secar. Se recristaliza de EtOH. Se seca, se pesa y se determina el rendimiento.
| ¡PELIGRO! «Realizar en vitrina, tanto la nitración (paso B) como la adición de amoniaco (paso C).» |
C) Preparación de la p-nitroanilina
La síntesis de la p-nitroanilina concluye con la desprotección del grupo amino. Para ello, la p-nitroacetanilida húmeda se coloca en un vaso de precipitados de 400 ml, y se forma con ella una pasta fina, añadiendo 100 ml de agua y agitando. Esta mezcla se pasa a un matraz de 250 ml, se le agregan 35 ml de HCl (conc.) y se le adapta al matraz de fondo redondo un refrigerante de reflujo.
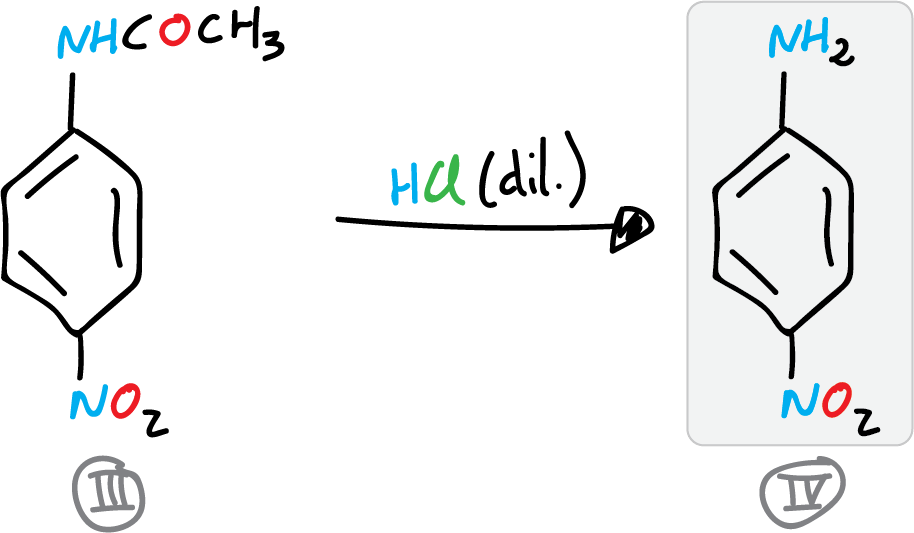
A continuación, se calienta a ebullición durante 35 min. Se deja enfríar el crudo de reacción a temperatura ambiente. Una vez enfriado el crudo de reacción, se vierte sobre un vaso de precipitados de 500 ml, con aprox. 50-75 g de hielo picado. La p-nitroanilina precipita alcalinizando la disolución mediante adición de amoniaco.
El precipitado se filtra a vacío en un Büchner, lavando con pequeñas porciones de agua. Se recristaliza en agua, decolorando con carbón activo (aprox. 0.5 g de sustancia en 40-50 ml de agua). Se seca, se pesa y se determina los rendimientos (parciales y totales).
Propiedades físico-químicas
La siguiente tabla recoge los datos de peso molecular (Mw), punto de fusión (P.F.) punto de ebullición (P.E.) y densidad de los reactivos y compuestos utilizados en este experimento de laboratorio.
| Name | Mw (g/mol) | M.p. (ºC) | B.p. (ºC) | Density (g/ml) |
| Acetanilida | 135.16 | 113-115 | 304 | - |
| Ácido acético | 60.05 | 16.2 | 118 | 1.049 |
| Anhídrido acético | 102.09 | -73.1 | 139.8 | 1.080 |
| Anilina | 93.13 | -6 | 184 | 1.022 |
| H2SO4 | 98.08 | 3 | - | 1.80-1.84 |
| HCl | 36.46 | -30 | >100 | 1.200 |
| HNO3 | 63.01 | - | 120.5 | 1.413 |
| NH3 | 17.03 | -78 | -33 | 0.590 |
| p-Nitroacetanilida | 180.16 | 213-215 | - | - |
| p-Nitroanilina | 138.12 | 146-149 | 260 | 1.440 |
GHS pictogramas
Los pictogramas de peligro forman parte del Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos (GHS) y se recogen en la siguiente tabla para los compuestos químicos utilizados en este experimento.
| Name | GHS |
| Acetanilida |  |
| Ácido acético |   |
| Anhídrido acético |    |
| Anilina |     |
| H2SO4 |  |
| HCl |   |
| HNO3 |   |
| NH3 |     |
| p-Nitroacetanilida |  |
| p-Nitroanilina |   |
Identificador Químico Internacional
Los identificadores IUPAC InChI key de los principales compuestos utilizados en este experimento se proporcionan para facilitar la nomenclatura y formulación de los compuestos químicos y la búsqueda de información en Internet de los mismos.
| Acetanilida | FZERHIULMFGESH-UHFFFAOYSA-N |
| Ácido acético | QTBSBXVTEAMEQO-UHFFFAOYSA-N |
| Anhídrido acético | WFDIJRYMOXRFFG-UHFFFAOYSA-N |
| Anilina | PAYRUJLWNCNPSJ-UHFFFAOYSA-N |
| H2SO4 | QAOWNCQODCNURD-UHFFFAOYSA-N |
| HCl | VEXZGXHMUGYJMC-UHFFFAOYSA-N |
| HNO3 | GRYLNZFGIOXLOG-UHFFFAOYSA-N |
| NH3 | QGZKDVFQNNGYKY-UHFFFAOYSA-N |
| p-Nitroacetanilida | NQRLPDFELNCFHW-UHFFFAOYSA-N |
| p-Nitroanilina | TYMLOMAKGOJONV-UHFFFAOYSA-N |
Volver a la página de prácticas de Síntesis Orgánica.
Catedrático de Química Orgánica en la Universidad de Granada, con una larga trayectoria en Química Computacional, en modelado y diseño molecular.
